

علم الكيمياء

تاريخ الكيمياء والعلماء المشاهير

التحاضير والتجارب الكيميائية

المخاطر والوقاية في الكيمياء

اخرى

مقالات متنوعة في علم الكيمياء

كيمياء عامة


الكيمياء التحليلية

مواضيع عامة في الكيمياء التحليلية

التحليل النوعي والكمي

التحليل الآلي (الطيفي)

طرق الفصل والتنقية


الكيمياء الحياتية

مواضيع عامة في الكيمياء الحياتية

الكاربوهيدرات

الاحماض الامينية والبروتينات

الانزيمات

الدهون

الاحماض النووية

الفيتامينات والمرافقات الانزيمية

الهرمونات


الكيمياء العضوية

مواضيع عامة في الكيمياء العضوية

الهايدروكاربونات

المركبات الوسطية وميكانيكيات التفاعلات العضوية

التشخيص العضوي

تجارب وتفاعلات في الكيمياء العضوية


الكيمياء الفيزيائية

مواضيع عامة في الكيمياء الفيزيائية

الكيمياء الحرارية

حركية التفاعلات الكيميائية

الكيمياء الكهربائية


الكيمياء اللاعضوية

مواضيع عامة في الكيمياء اللاعضوية

الجدول الدوري وخواص العناصر

نظريات التآصر الكيميائي

كيمياء العناصر الانتقالية ومركباتها المعقدة


مواضيع اخرى في الكيمياء

كيمياء النانو

الكيمياء السريرية

الكيمياء الطبية والدوائية

كيمياء الاغذية والنواتج الطبيعية

الكيمياء الجنائية


الكيمياء الصناعية

البترو كيمياويات

الكيمياء الخضراء

كيمياء البيئة

كيمياء البوليمرات

مواضيع عامة في الكيمياء الصناعية

الكيمياء الاشعاعية والنووية
التفاعلات المهمة للاحماض الامينية والببتيدات
المؤلف:
د. طارق يونس احمد / د. لؤي عبد علي الهلالي
المصدر:
الكيمياء الحياتية
الجزء والصفحة:
ج 1 ص 123- 130
2023-11-13
2452
1- التفاعل مع الكاشف ننهايدرين Ninhydrin
الأحماض الأمينية جميع تتفاعل مع الننهايدرين لتكوين الألديهايد وثاني أوكسيد الكاربون CO2 وأمونيا ماعدا الحامض الأميني برولين وهيدروكسي برولين. ان كمية CO2 المتحررة من هذا التفاعل يمكن ان تستعمل للتقدير الكمي للأحماض الأمينية. اما جزيئة الأمونيا المتكونة في التفاعل نفسه فأنها ترتبط بجزيئتين من ننهايدرين لتكون مركباً أزرق اللون يقاس عند طول موجي 570 نانوميتر ، وهذا يشكل الأساس للطريقة اللونية المستعملة في التقدير الكمي للأحماض الأمينية.
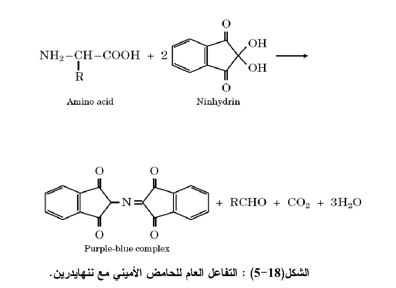
2- التفاعل مع حامض النتروز Nitrous acid
يعد هذا التفاعل الأساسي لطريقة الباحث فان سلايك Van Slyke المستخدم في تقدير مجموعة الأمين للأحماض الأمينية كما في المعادلة أدناه، وان غاز النتروجين المتحرر في هذا التفاعل يجمع ويقدر حجمه.
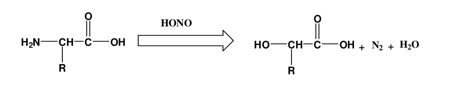
3- التفاعل مع 1- فلورو 2، 4 - ثنائي نايتروبنزين (1-Flouro 2,4-dinitrobenzene (FDNB) (کاشف سانگر Sanger reagent)
لقد وجد الباحث سأذكر أن المجموعة الأمينية في الببتيد تتفاعل مع كاشف سانكر (FDNB) لتعطي مركباً مشتقاً أصفر اللون والذي عند تعامله مع حامض الهيدروكلوريك تنكسر الأصرة التي ترتبط مع 4،2 ثنائي نايتروفينايل ومجموعة الأمين الألفا للحامض الأميني في النهاية النيتروجينية إذ تبقى ثابتة ضد التحلل المائي الحامضي والتي من الممكن تشخيصها معتمدة على نوع الحامض الأميني المرتبط (الشكل 20-5 ).
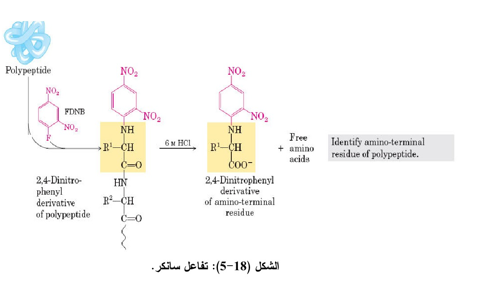
4- التفاعل مع ليثيوم بوروهيدريد Lithium borohydride
يتفاعل هذا المركب مع النهاية الكاربوكسيلية للحامض الأميني والذي يحوله الى كحول أميني عند التحلل المائي للسلسلة الببتيدية، فالنواتج تحتوي على جزيئة واحدة من الكحول الأميني كما في المعادلة أدناه معتمداً على نوع الحامض الأميني الموجود في النهاية الكاربوكسيلية، ومن الممكن تشخيص هذه المكونات بالطرائق الكروموتوكرافية.
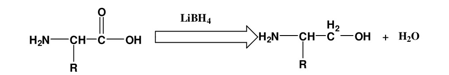
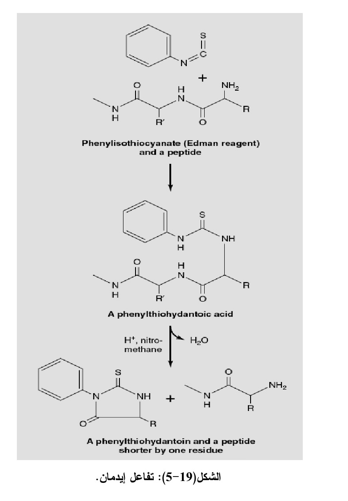
5- التفاعل مع أيزوثايوسيانات (كاشف إدمان Edman reagent)
يستخدم هذا الكاشف لمعرفة الحامض الأميني في النهاية الأمينية، اذ يتحد مع مجموعة ألفا- أمين للببتيد منتجاً فينايل ثايو كار بوميل Phenyl thiocarbonyl الشكل (19-5) عند التحلل الحامضي لهذا المركب ينتج مركباً حلقياً يسمى فنيل ثايوهاي دانتوينPhenyl thiohydantion يمكن تشخيصه بوساطة الكروماتوكرافيا أو المطياف اللوني ومعرفة الحامض الأميني في الطرف النيتروجيني وبالاعتماد على المحاليل القياسية للأحماض الأمينية المحضرة يمكن أيجاد نوعية وكمية الأحماض الأمينية المتحررة بالمقارنة مع المحاليل القياسية للأحماض الأمينية. وهذه الطريقة هي الأساس في مبدأ جهاز إدمان لإيجاد نوعية وتسلسل الأحماض الأمينية في الببتيدات الناتجة من تحلل البروتين.
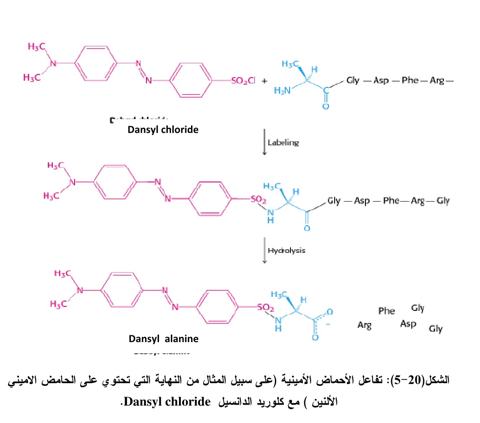
6- التفاعل مع كلوريد الدانسيل Dansyl Chloride
نظراً لكون مجموعة الدانسيل (Dimethyl amino naphthalene -5-sulfonyl chloride-1) تعطي فورة Fluorescent لذا من الممكن أيجاد وقياس كميات قليلة من مشتقات الدانسيل Dansyl derivatives للحامض الأميني في النهاية النيتروجينية، وتعد هذه الطريقة من أكثر الطرائق دقة وحساسية لمعرفة النهاية الأمينية للبروتينات (الشكل 20-5)
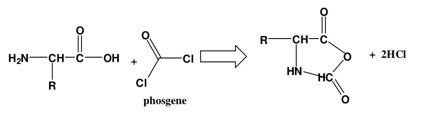
7 - التفاعل مع الفوسجين Phosgene
يتفاعل الفوسجين مع المجاميع الأمينية لتكوين N-carboxy anhydrides كما في المعادلة الآتية:
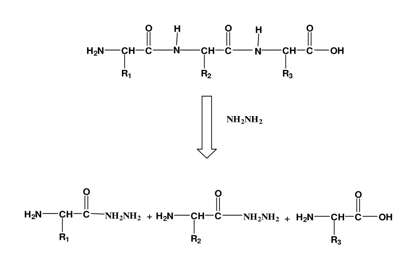
8- التفاعل مع الهيدرازين
يتفاعل الهيدازين مع الببتيدات فيعمل على تكسير جميع الأواصر الببتيدية ماعدا الأحماض الأمينية في النهاية الكاربوكسيلية التي تتحول الى الهايدرازايد ويظهر الحامض الأميني في النهاية الكاربوكسيلية بوصفه حامضاً أمينياً حراً والتي من الممكن تشخيصه كروموتوكرافياً كما في المعادلة الآتية:
9- التفاعل مع بروميد السيانوجين Cyanogen bromide
يستعمل بروميد السيانوجين لغرض التحلل الجزئي المائي للأواصر الببتيدية في مواقع الحامض الأميني مثيونين Methionine الذي يتحول الى لاكتون الهوموسيرين Homoserine lactone في النهاية الكاربونية كما هو موضح في التفاعل الأتي :

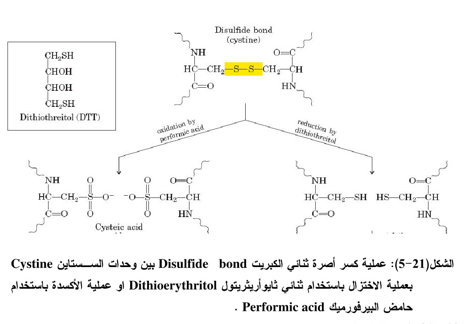
10- كسر أواصر ثنائي الكبريت Disulfide bonds
يمكن كسر أواصر ثنائي الكبريت بين وحدات المستين باختزالهم والذي يستخدم فيها غالباً مادة -2- ميركبتو إيثانول Mercaptoethanol-2 ، أو ثنائي ثايوثيريتول Dithiothreitol او ثنائي ثايو أريثريتول Dithioerythritol (کاشف کلیلاند (Cleland reagent) ويمكن كذلك كسر الأصرة بوساطة أكسدتها باستخدام حامض البيرفورميك Performic acid وتحويلها الى حامض الستيك (الشكل 21-5).
11- التفاعل مع الإنزيمات
هناك العديد من الإنزيمات التي تعمل على تكسير الأواصر الببتيدية وفصل الأحماض الأمينية استناداً إلى نوعية الإنزيم المستخدم ويمكن تقسيم الإنزيمات المحللة للبروتين الى:
أ- إندوببتايديز Endopeptidases
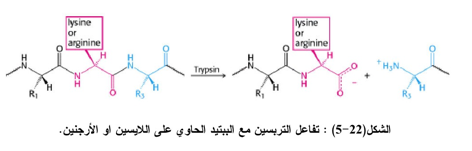
الإندوببتايديز من الإنزيمات التي تهاجم الأواصر الببتيدية الداخلية فضلاً عن الأواصر الببتيدية الطرفية في سلسلة متعدد الببتيد ويطلق عليها البروتييز Proteases مثل الببسين Pepsin والإيلاستيز Elastase والتربسين Trypsin (الشكل 22-5) والكيموتريسين Chymotrypsin في اللبائن أو البابايين Papain والفيسين Fisin في النباتات. وفي ما يأتي جدول (5-5) لبعض أنواع الإنزيمات المحللة للببتيدات.

ب- الإكسوببتايديز Exopeptidases
الإكسوببتايديز وهي الإنزيمات التي تهاجم الأواصر الببتيدية الطرفية فقط لسلاسل الببتيد بحيث تنزع الأحماض الأمينية بالتتابع ومنها كاربوكسي ببتايديز Carboxy peptidases الذي يعمل على الأواصر الببتيدية من الطرف الكاربوكسيلي (C-terminal) للببتيد قليل الوحدات Oligopeptides مثل الببتيد الثلاثي والرباعي، أو الببتيدات المتعددة، وإنزيمات أمينو ببتايديز Aminopeptidases وهي الإنزيمات التي تعمل على مهاجمة الأواصر الببتيدية من النهاية الأمينية. وتوجد أيضاً إنزيمات ثنائي ببتيديز Dipeptidases التي تعمل على الببتيدات الثنائية أي تعمل على الطرف الكاربوكسيلي والطرف النيتروجيني.