

علم الكيمياء

تاريخ الكيمياء والعلماء المشاهير

التحاضير والتجارب الكيميائية

المخاطر والوقاية في الكيمياء

اخرى

مقالات متنوعة في علم الكيمياء

كيمياء عامة


الكيمياء التحليلية

مواضيع عامة في الكيمياء التحليلية

التحليل النوعي والكمي

التحليل الآلي (الطيفي)

طرق الفصل والتنقية


الكيمياء الحياتية

مواضيع عامة في الكيمياء الحياتية

الكاربوهيدرات

الاحماض الامينية والبروتينات

الانزيمات

الدهون

الاحماض النووية

الفيتامينات والمرافقات الانزيمية

الهرمونات


الكيمياء العضوية

مواضيع عامة في الكيمياء العضوية

الهايدروكاربونات

المركبات الوسطية وميكانيكيات التفاعلات العضوية

التشخيص العضوي

تجارب وتفاعلات في الكيمياء العضوية


الكيمياء الفيزيائية

مواضيع عامة في الكيمياء الفيزيائية

الكيمياء الحرارية

حركية التفاعلات الكيميائية

الكيمياء الكهربائية


الكيمياء اللاعضوية

مواضيع عامة في الكيمياء اللاعضوية

الجدول الدوري وخواص العناصر

نظريات التآصر الكيميائي

كيمياء العناصر الانتقالية ومركباتها المعقدة


مواضيع اخرى في الكيمياء

كيمياء النانو

الكيمياء السريرية

الكيمياء الطبية والدوائية

كيمياء الاغذية والنواتج الطبيعية

الكيمياء الجنائية


الكيمياء الصناعية

البترو كيمياويات

الكيمياء الخضراء

كيمياء البيئة

كيمياء البوليمرات

مواضيع عامة في الكيمياء الصناعية

الكيمياء الاشعاعية والنووية
العوامل المؤثرة على حركية تفاعلات الأكسدة الضوئية
المؤلف:
مثنى صالح مشكور الجبوري
المصدر:
دراسة و معالجة المياه الصناعية المصرفة التابعة للشركة العامة للصناعات النسيجية في الحلة
الجزء والصفحة:
ص 37-39
2024-01-28
1016
هنالك بعض العوامل تؤثر على عملية التحفيز غير المتجانس في التفاعلات الضوئية ويمكن توضحيها كالاتي :
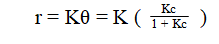
إذ إن K هو ثابت معدل سرعة التفاعل و K هو ثابت امتزاز المركب و C التركيز الابتدائي للمادة الأساس في المحاليل المخففة فإن KC <<1 . لذا فان التفاعل من المرتبة الأولى . أما في المحاليل المركزة فإن KC>>1 وأن هذا التفاعل من المرتبة
الصفرية(3-4).
3.تأثير درجة الحرارة والرقم الهيدروجيني :إن معظم التفاعلات الضوئية غير حساسة للتغيرات الطفيفة في درجات الحرارة وحالات قليلة جداً بنيت تأثير أرينس خلال عملية التكسير الضوئي(5). في حين أن الرقم الهيدروجيني للمحاليل المائية تؤثر على حجم الجزئيات وشحنة السطح ومواقع حافة الحزمة لـTiO2 بسبب خواصة الامفوتيرية(6) . إن شحنة نقطة الصفر (Zero Point Charge) تمثل الرقم الهيدروجيني لـTiO2 عندما يكون سطح الأوكسيد غير مشحون وتكون بحدود 7 وعند الزيادة أو النقصان عن هذا فإن العامل المحفز يكون إما سالب وأما موجب الشحنة وكما في المعادلات الاتية :
TiOH+2 TiOH + H+ ……………………(1-31)
TiOH TiO- + H+ ………………………(1-32)
وبذلك فإن الأكسدة الضوئية المحفزة للمركبات العضوية تتأثر بالرقم الهيدروجيني .
4.الأيونات اللأعضوية : تؤثر بعض الايونات السالبة في المياه الطبيعة أو الملوثة مثل ( الكلوريدات والبروميدات والكبرتيتات والفوسفات ) بشكل مثبط لعملية التكسير الضوئي إذا ما أتحدت مع TiO2 أو اقتربت من سطحة(7-8) . زيادة على الفعالية الكيميائية للأيونات السالبة اتجاه TiO2 فإن الرقم الهيدروجيني يبين خواص الأيونات المؤثرة , إذ إن معدل سرعة التكسير الضوئي لمركبات مختلفة تثبطت بوجود الكلوريد عند pH = 3-4 (9), فبوجود الوسط الحامضي تكون الاشكال الهندسية لـTiO2 أما TiOH2+ أو TiOH وعند اقتراب آيونات الكلوريد من المراكز الفعالة فإنها تقلل من معدل سرعة التفاعل , أما بوجود الوسط القاعدي فإن اقتراب أيونات الكلوريد لا تتملك أي تايثر تثبيطي لوجود شحنة سالبة على سطح العامل المحفز و كما هو الحال بوجود أيونات النتريت .
5.شدة الضوء : تتناسب سرعة التفاعلات الضوئية المحفزة مع شدة الضوء وذلك بتناسب سرعة التفاعلات الضوئية مع الجذر التربيعي لشدة الضوء عند الشدة الفعالة(10).
6. الأوكسجين : تعتمد فعالية ومعدل سرعة التفاعل الضوئي المحفز لتكسير المركبات العضوية على وجود الاوكسجين أو اضافة بعض المؤكسدات مثل
(Peroxy disulfate or Peroxides)(11). أن جزئية الاوكسجين تعمل كمصيدة لألكترون حزمة التكافؤ وإن تركيز الاوكسجين يعتمد على ما يتطلب من الأوكسجين للأمتزاز أو الاستهلاك في الضوء أو الظلام .
7. الطول الموجي : يمثل التغير في معدل سرعة التفاعلات الضوئية المحفزة دالة للطول الموجي بالاعتماد على الطيف الامتصاصي للعامل المحفز من خلال طاقة فجوة الحزمة , وبما أن TiO2 و ZnO يملكان طاقة فجوة حزمة مقدارها (3,2) الكترون فولت لذا فهو يمتص في المنطقة القريبة من الأشعة فوق البنفسجية (max-UV) وعند طول موجي (387)نانوميتر وبذلك يجب التأكد من أن المتفاعلات لا تمتص عند هذا الطول الموجي .
8. الامتزاز : يعد أمتزاز المركبات العضوية على سطح جزيئات شبه الموصل من أهم الاعتبارات في تفاعل الأكسدة الضوئية المحفزة, إذ يبين Langmiur العلاقة بين معدل سرعة تفاعل التكسير والتركيز الابتدائي لمركب العضوي وبذلك فأن الامتزاز يطيع قانون التفاعلات الضوئية المحفزة .
---------------------------------------------------------------------------------------------------
1- J. Gimenez, D. Cureo, M. A. Queral, Catalysis Today, 54 ( 2-3), 243 ( 1999 ).
2- J. P. Percherancier, R. Chapelon, B. Buyet, Journal of Photochemistry and Photobiology A: Chemistry, 87, 266 (1995).
3- J. M. Herrmann, Catalysis Today, 53, 129 ( 1999 ).
4- I. Arslan, I. A. Balcioglu, D. W. Banhemann, Applied Catalysis B: Environmental, 26, 206 ( 2000 ).
5- T. Zhang, Journal of Photo Chemistry and Photobiology A: Chemistry, 104, 172 ( 2001 ).
6- P. Fernandez–Ibanez, F. J. de-Las Nieves, S. Malato, Journal of Colloid and Interface Science, 227, 516 ( 2000 ).
7- E. Pelizzetti, Solar Energy Materials and Solar Cells, 38, 457 (1995).
8- K. H. Wang, Chemosphere, 40, 394 ( 2000 ).
9- K. H. Wang, Applied Catalysis B: Environmental, 21, 8 (1999 ).
10- G. Al Sayyed , J. C. D’Oliveira , P. Pichat , Journal of Photochemistry and Photo Biology A: Chemistry, 58, 114 ( 1991 ) .
11- Y. wang , C. S. Hong , water research , 34 ( 10 ) ,2797 ( 2000 ).