

علم الكيمياء

تاريخ الكيمياء والعلماء المشاهير

التحاضير والتجارب الكيميائية

المخاطر والوقاية في الكيمياء

اخرى

مقالات متنوعة في علم الكيمياء

كيمياء عامة


الكيمياء التحليلية

مواضيع عامة في الكيمياء التحليلية

التحليل النوعي والكمي

التحليل الآلي (الطيفي)

طرق الفصل والتنقية


الكيمياء الحياتية

مواضيع عامة في الكيمياء الحياتية

الكاربوهيدرات

الاحماض الامينية والبروتينات

الانزيمات

الدهون

الاحماض النووية

الفيتامينات والمرافقات الانزيمية

الهرمونات


الكيمياء العضوية

مواضيع عامة في الكيمياء العضوية

الهايدروكاربونات

المركبات الوسطية وميكانيكيات التفاعلات العضوية

التشخيص العضوي

تجارب وتفاعلات في الكيمياء العضوية


الكيمياء الفيزيائية

مواضيع عامة في الكيمياء الفيزيائية

الكيمياء الحرارية

حركية التفاعلات الكيميائية

الكيمياء الكهربائية


الكيمياء اللاعضوية

مواضيع عامة في الكيمياء اللاعضوية

الجدول الدوري وخواص العناصر

نظريات التآصر الكيميائي

كيمياء العناصر الانتقالية ومركباتها المعقدة


مواضيع اخرى في الكيمياء

كيمياء النانو

الكيمياء السريرية

الكيمياء الطبية والدوائية

كيمياء الاغذية والنواتج الطبيعية

الكيمياء الجنائية


الكيمياء الصناعية

البترو كيمياويات

الكيمياء الخضراء

كيمياء البيئة

كيمياء البوليمرات

مواضيع عامة في الكيمياء الصناعية

الكيمياء الاشعاعية والنووية
استعمالات المركبات التساهمية (Coordination compounds)
المؤلف:
د.عبدالله محمود ابو الكباش
المصدر:
الكيمياء التحليلية المفاهيم الاساسية في التحليل التقليدي والالي
الجزء والصفحة:
ص 110-111
2024-02-06
973
تستخدم المركبات التساهمية في العديد من التطبيقات، ولقد أمكن تحضير بعض المعطيات (ligands) التي تتفاعل بشكل انتقائي لأنواع معينة من التطبيقات سنذكر فيما يلي بعضها :
1- تكوين مركبات ملونة ، وهذه تساعد على الكشف عن وجود بعض أيونات المعادن في العينات المراد تحليلها، ويمكن أيضاً معرفة تركيز هذه الأيونات فمثلاً مركب phenanthroline-1,10 يمكن استخدامه للكشف عن أيون الحديد الثنائي (II)Fe، حيث يتكون معقد ذو لون أحمر يدل على وجود (Fe(II ، وفي حالة غياب هذا الأيون يبقى المحلول عديم اللون.
2 - تستخدم المركبات التساهمية كحاجب masking agent) لبعض الأيونات التي تؤدي إلى تداخل Interference حين تحليل بعض المواد أو الأيونات في عينات معينة فمثلا عند تعيين أيون النحاس بتفاعله مع أيون الأيوديد -I لينتج اليود 2I، وهذا يمكن معايرته ومن ثم معرفة تركيز أيونات النحاس في العينة. وفي حالة وجود أيون الحديد الثلاثي Fe+3 الذي يتفاعل هو الآخر مع أيون الايوديد، ومن ثُمَّ يؤدي إلى تداخل، ولحجب تأثير أيون الحديد Fe3يضاف إلى المحلول ملح الفلوريد القابل للذوبان، حيث يتأين Fe+3 ويعطي أيونات الفلوريد -F وهذه تعمل معقداً مع أيون Fe+3
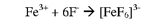
من ثُمَّ يتم التغلب على تداخل أيون الحديد Fe+3.
3- يستخدم العديد من المعطيات عديدة الأسنان (polydentate ligands) في معايرة أيونات المعادن، وهذه المعطيات تتفاعل مع أيونات المعادن بشكل سريع وضمن خطوة واحدة بعكس المعطيات أحادية السن التي تتفاعل ضمن عدة خطوات، مما يجعل استخدامها كمواد للمعايرة أمراً غير ممكن. ومن بين المعطيات عددية الأسنان يُعدُّ (Ethylenediamintetra acetic acid (EDTA أحد أهم المعطيات التي تستخدم في معايرة أيونات المعادن. وهذا المركب هو سداسي الأسنان (hexadentate)، حيث يحتوي على أربع ذرات أكسجين وذرتي نيتروجين، وجميعها تساهم بإلكترونات حرة، هذا بالإضافة إلى أن هذا المركب يُعَدُّ حمضاً رباعيا tetraprotic acid ، ويوجد في أشكال مختلفة حسب درجة حمضية المحلول، وتشمل هذه الأشكال -4H4Y ، H3Y- ، H2Y-2 ، HY-3 ، Y حيث لا ترمز إلى بقية الجزيء بدون البروتونات. وتجدر الإشارة إلى أن كل واحد من هذه الأشكال قد يتفاعل مع أيون معدني، ويكون معقداً لذا لا بد من مراعاة استخدام منظمات درجة الحموضة Buffers حين إجراء المعايرة باستخدام هذا المركب.