

علم الكيمياء

تاريخ الكيمياء والعلماء المشاهير

التحاضير والتجارب الكيميائية

المخاطر والوقاية في الكيمياء

اخرى

مقالات متنوعة في علم الكيمياء

كيمياء عامة


الكيمياء التحليلية

مواضيع عامة في الكيمياء التحليلية

التحليل النوعي والكمي

التحليل الآلي (الطيفي)

طرق الفصل والتنقية


الكيمياء الحياتية

مواضيع عامة في الكيمياء الحياتية

الكاربوهيدرات

الاحماض الامينية والبروتينات

الانزيمات

الدهون

الاحماض النووية

الفيتامينات والمرافقات الانزيمية

الهرمونات


الكيمياء العضوية

مواضيع عامة في الكيمياء العضوية

الهايدروكاربونات

المركبات الوسطية وميكانيكيات التفاعلات العضوية

التشخيص العضوي

تجارب وتفاعلات في الكيمياء العضوية


الكيمياء الفيزيائية

مواضيع عامة في الكيمياء الفيزيائية

الكيمياء الحرارية

حركية التفاعلات الكيميائية

الكيمياء الكهربائية


الكيمياء اللاعضوية

مواضيع عامة في الكيمياء اللاعضوية

الجدول الدوري وخواص العناصر

نظريات التآصر الكيميائي

كيمياء العناصر الانتقالية ومركباتها المعقدة


مواضيع اخرى في الكيمياء

كيمياء النانو

الكيمياء السريرية

الكيمياء الطبية والدوائية

كيمياء الاغذية والنواتج الطبيعية

الكيمياء الجنائية


الكيمياء الصناعية

البترو كيمياويات

الكيمياء الخضراء

كيمياء البيئة

كيمياء البوليمرات

مواضيع عامة في الكيمياء الصناعية

الكيمياء الاشعاعية والنووية
Getting names from formulas and formulas from names
المؤلف:
John T. Moore, EdD
المصدر:
Chemistry Essentials For Dummies
الجزء والصفحة:
p 67
3-1-2017
1575
Getting names from formulas and formulas from names
Sometimes figuring out the charge on an ion can be a little challenging (and fun), so take a look at how to name FeNH4(SO4)2. I show you earlier the sulfate ion has a 2– charge, and from the formula you can see that there are two of these ions. Therefore, you have a total of four negative charges. The ammonium ion has a 1+ charge, so you can figure out the charge on the iron cation:
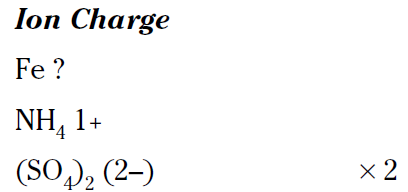
Because you have a 4– charge for the sulfates and a 1+ for the ammonium, the iron must be a 3+ to make the compound neutral. So the iron is in the iron (III), or ferric, oxidation state. You can name the compound:
FeNH4(SO4)2: Iron (III) ammonium sulfate, or ferricammonium sulfate And finally, if you have the name, you can derive the formulaand the charge on the ions. For example, suppose that you’re given the name cuprous oxide. You know that the cuprous ion is Cu+ and the oxide ion is O2–. Applying the crisscross rule (from the earlier section “Using the crisscross rule”), you get the following formula:
Cuprous oxide: Cu2O