


 الفيزياء الكلاسيكية
الفيزياء الكلاسيكية
 الكهربائية والمغناطيسية
الكهربائية والمغناطيسية
 علم البصريات
علم البصريات
 الفيزياء الحديثة
الفيزياء الحديثة
 النظرية النسبية
النظرية النسبية
 الفيزياء النووية
الفيزياء النووية
 فيزياء الحالة الصلبة
فيزياء الحالة الصلبة
 الليزر
الليزر
 علم الفلك
علم الفلك
 المجموعة الشمسية
المجموعة الشمسية
 الطاقة البديلة
الطاقة البديلة
 الفيزياء والعلوم الأخرى
الفيزياء والعلوم الأخرى
 مواضيع عامة في الفيزياء
مواضيع عامة في الفيزياء|
أقرأ أيضاً
التاريخ: 12-1-2023
التاريخ: 2023-10-12
التاريخ: 30-1-2023
التاريخ: 17-5-2016
|
الذرة هي مجموعة من الجسيمات المتناهية في الدقة وهذه الجسيمات تتكون من نواة موجبة الشحنة، وتحتوي في الغالب على البروتونات (موجبة الشحنة)، والنيترونات (المتعادلة). كما يوجد أيضًا عدد من الإلكترونات (سالبة الشحنة) التي تعادل الشحنة الموجبة في النواة (انظر: الشكل رقم 1). وتدور الإلكترونات في مستويات مختلفة تعرف بمستويات الطاقة، حيث يحمل المستوى الأول إلكترونين فقط، في حين يحمل المستوى الثاني ثمانية إلكترونات (انظر الشكل رقم 2)، أما المستوى الثالث فهو يحمل 18 إلكترونا. ولكل مستوى طاقة أساسي، مستويات فرعية يرمز لها بالرموز s،p،d،f (انظر: الشكل رقم 3). وتكون الذرات في الغالب متعادلة كهربيًّا؛ لأن عدد الإلكترونات السالبة يساوي عدد البروتونات الموجبة، ويمكن للذرة أن تتحول إلى أيون موجب، وذلك عندما تفقد إلكترونًا أو أكثر عند التفاعل الكيميائي، كما يمكن أن تتحول إلى أيون سالب، وذلك عندما تكتسب إلكترونًا أو أكثر، وذلك بحسب قيمة الشحنة التي تفقدها أو تكتسبها.
ونذكر بعض المفاهيم الأساسية التي يفترض إدراكها وفهمها لدى القارئ الكريم:
1 - تتكون المادة من وحدات بناء أساسية تسمى الذرات.
2- التركيب الذري للمادة له دور أساس في تحديد خصائص المادة.
3- تتكون الذرة من نواة موجبة الشحنة (بداخلها البروتونات الموجبة والنيوترونات المتعادلة)، وتحيط بها جسيمات سالبة الشحنة تسمى الإلكترونات.
4- تتوزع الإلكترونات حول النواة في مستويات طاقة محددة، وتعتمد قوة ارتباط الإلكترونات في مستويات الطاقة على بعدها عن النواة.
5- تسمى الإلكترونات الموجودة في مستويات الطاقة الأخيرة إلكترونات التكافؤ.
6- يمكن لبعض الإلكترونات الموجودة في مستوى الطاقة الأخير لبعض الذرات أن تتحرر نظرا لضعف ارتباطها بالنواة.
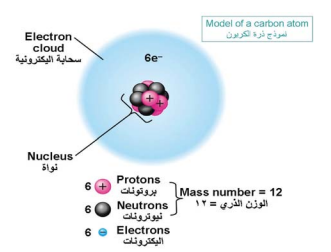
شكل رقم (1) أنموذج ذرة الكاربون.
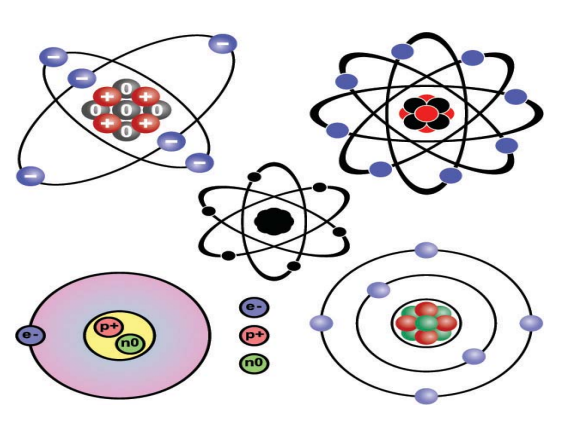
شكل رقم (2) الالكترونات حول النواة لذرة الكاربون.
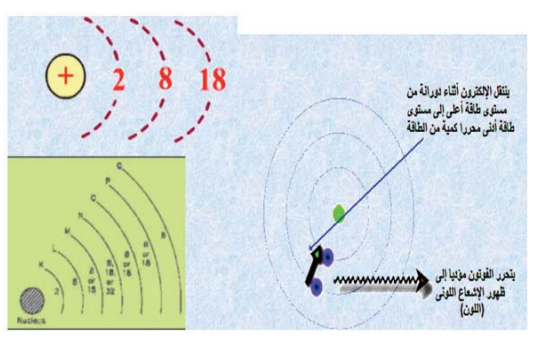
شكل رقم (3) توزيع الالكترونات في مستويات الطاقة.



|
|
|
|
دراسة تحدد أفضل 4 وجبات صحية.. وأخطرها
|
|
|
|
|
|
|
العتبة العباسية تحتفي بذكرى ولادة الإمام الجواد (عليه السلام) في مشاتل الكفيل
|
|
|