


 علم الكيمياء
علم الكيمياء 
 الكيمياء التحليلية
الكيمياء التحليلية 
 الكيمياء الحياتية
الكيمياء الحياتية 
 الكيمياء العضوية
الكيمياء العضوية 
 الكيمياء الفيزيائية
الكيمياء الفيزيائية
 الكيمياء اللاعضوية
الكيمياء اللاعضوية 
 مواضيع اخرى في الكيمياء
مواضيع اخرى في الكيمياء
 الكيمياء الصناعية
الكيمياء الصناعية |
أقرأ أيضاً
التاريخ: 2025-04-28
التاريخ: 11-9-2020
التاريخ: 2023-08-29
التاريخ: 3-11-2019
|
1- من الألكينات: هناك بعض الطرق التي يمكن اتباعها لتحضير بعض الكحولات مثل إضافة البورون إلى الألكينات وكذلك أكسدتها بواسطة البرمنجنات أو بواسطة إضافة مركبات الزئبق وانتزاعها وإضافة عناصر الماء إليها، وهذه طرق سبق وأن عرفناها تحت بحث الألكينات
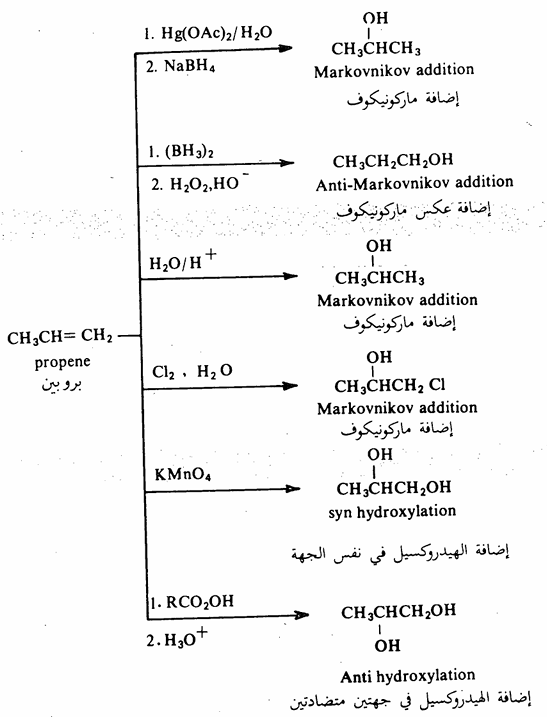
يضاف ثنائي البوران إلى الألكينات ليتكون إثر ذلك مركبات ثلاثي ألكيل بوران. وهذا التفاعل له أهميته المخبرية حيث يعتبر ركيزة جيدة كي يتبناه دارس الكيمياء العضوية كتفاعل شائع لتحضير الكحولات. فإذا ما عومل ناتج إضافة ثنائي البوران إلى الألكينات (ثلاثي ألكيل (بوران بفوق أكسيد الهيدروجين في الوسط القلوي ينشأ عندئذ الكحول، على سبيل المثال

وكما يظهر من التفاعل أعلاه أنه يتم على خطوتين، والنتيجة النهائية هي إضافة عناصر الماء على ذرتي كربون الرابطة المضاعفة. ويشار إلى مثل هذا التفاعل ككل Hydroxylation-oxidation. ونورد الآن المزيد من الأمثلة لتحضير الكحولات وفقاً لهذه الطريقة.
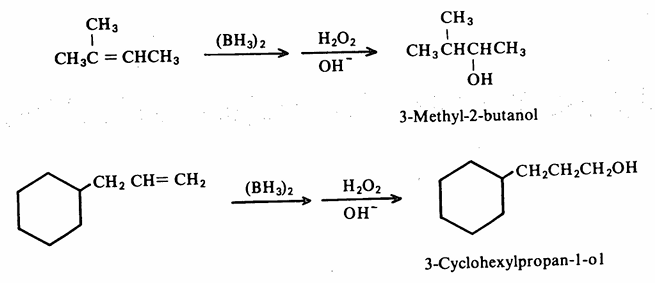
وتجدر الإشارة إلى أن هذه الإضافة على ذرتي كربون الرابطة المضاعفة كما يظهر من المثالين السابقين - تحدث عكس قاعدة ماركونيكوف ولا تحدث إعادة ترتيب في إضافة البورون إلى الألكين وعليه فإن ذلك يجعل لهذه الطريقة ميزة جيدة على تفاعلات الإضافة الأخرى والتي تكون في العادة مصحوبة ببعض النواتج غير المرغوب فيها. أما فيما يتعلق بالكيمياء الفراغية لتفاعل إضافة البورون والأكسدة فيمكن إدراكه من التفاعل التالي حيث تتم الإضافة على نفس الجانب
."Syn addition"
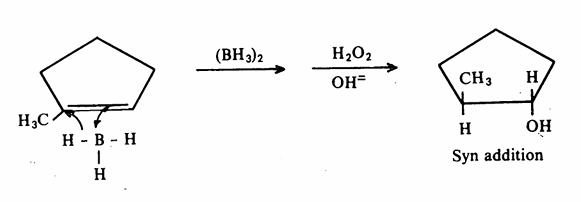
2- من هاليدات الألكيل تتحلل هاليدات الألكيل بالماء إلى الكحولات المطابقة، ولكن تطبيق هذه الطريقة في المختبر لتحضير الكحولات محدود نظراً لأن هاليدات الألكيل باهظة الثمن. أضف إلى ذلك أن أفضل الطرق لإصطناع هاليدات الألكيل هي من الكحولات وقد تم عرض هذه الطريقة في الفصل السادس. وتتمثل هذه الطريقة لتحضير الكحولات بالمعادلات العامة التالية:
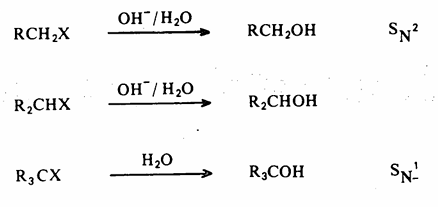
3-اختزال مركبات الكربونيل:
أ- اختزال الالدهايدات والكيتونات
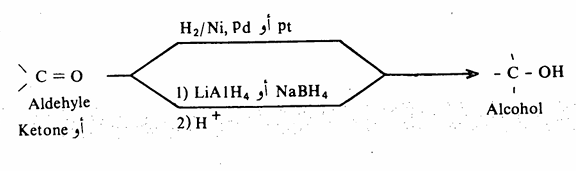
ب- اختزال الحموض الكربوكسيلية ومشتقاتها
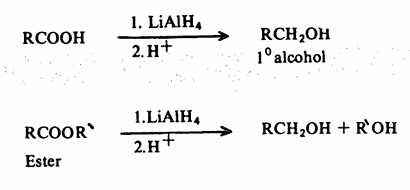
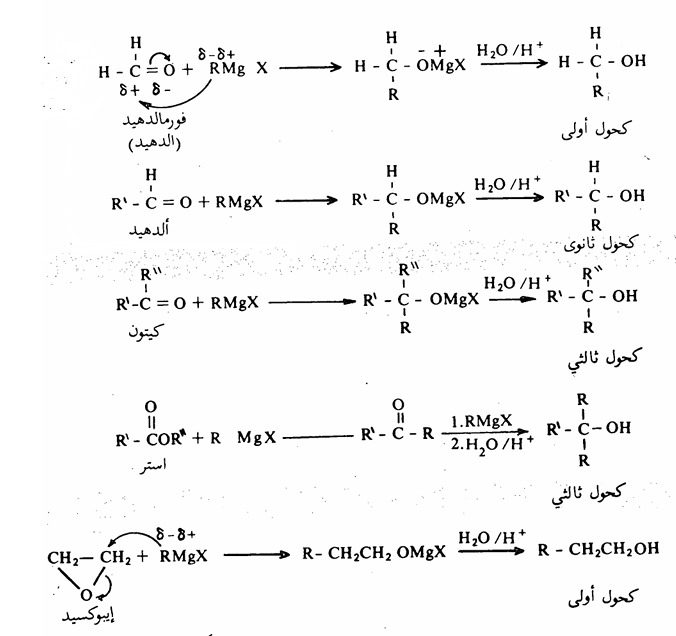
4- تفاعل كاشف جرينارد مع الألدهيدات والكيتونات والأسترات والأيبوكسيدات تأخذ ذرة الكربون المرتبطة بالأكسجين في هذه المركبات الشحنة الموجبة الجزئية وعليه فهي قابلة للهجوم النيكلوفيلي من المجموعة الهيدروكربونية کاشف جرينارد ذات الطبيعة النيكلوفيلية نظراً للفارق في السالبية الكهربية بين المغنسيوم وذرة الكربون (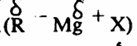 ) وينشأ عن هذا الهجوم النيكلوفيلي نزوح زوج الكتروني إلى ذرة الأكسجين ويتشكل عندئذ أيونات الالكوكسيدات (أملاح الكحولات) ومن ثم الحصول على الكحول الحر بمعاملة هذه الأملاح بالماء في وجود حمض معدني.
) وينشأ عن هذا الهجوم النيكلوفيلي نزوح زوج الكتروني إلى ذرة الأكسجين ويتشكل عندئذ أيونات الالكوكسيدات (أملاح الكحولات) ومن ثم الحصول على الكحول الحر بمعاملة هذه الأملاح بالماء في وجود حمض معدني.
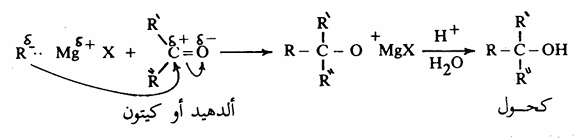
ويعتمد نوع الكحول التي يمكن تحضيره وفقاً لهذه الطريقة على نوع المركب الكربونيلي الذي يتفاعل مع كاشف جرينارد. فالكحولات الأولية تنشأ من الفورمالدهيد ، في حين أن الألدهيدات الأخرى تتفاعل مع الكاشف لتعطي كحولات ثانوية أما الكحولات الثالثية فتتكون من الكيتونات أو الاسترات، هذا ويتفاعل كاشف جرينارد مع الايبوكسيد ليعطي كحول أولي كما يتبين من المعادلات التالية:
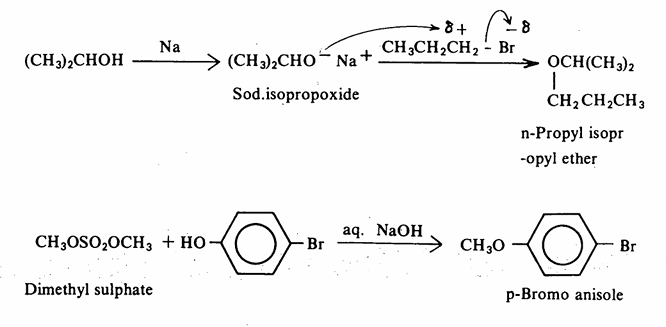
5- تحضير وليمسون Williamson's synthesis : يتم وفقا لهذه الطريقة تحضير الايثرات المتماثلة وغير المتماثلة وذلك من معاملة الملح الصوديومي للكحولات (أيون الكوكسيد alkoxide ion)، أو الملح الصوديومي للفينولات، بهاليد الألكيل عن طريق إستبدال نيكليوفيلي من الدرجة الثانية (SN2). يمكن الحصول على الملح الصوديومي للكحولات بمعاملة الكحول بمعدن الصوديوم. أما الملح الصوديومي للفينولات فيتم الحصول عليه بمعاملة الفينول بهيدروكسيد الصوديوم لأن الفينولات أكثر حمضية من الكحولات هذا ويمكن استخدام كبريتات ثنائي ألكيل بدلاً من هاليدات الألكيل فهذه الاسترات لها فعالية شديدة. وتجدر الإشارة إلى أن كبريتات ثنائي الميثل تستخدم على نطاق واسع في الكيمياء العضوية كعامل مثيله لإدخال مجموعة ميثل إلى مركب آخر بدلاً . من هاليدات الميثل الباهظة الثمن، كذلك فإن أيون الكوكسيد (الملح الصوديومي للكحولات) يمكن أن يكون مشتقاً من كحول أولي أو ثانوي أو ثالثي، بينما هاليد الألكيل لان وأن يكون أولياً لأن كلا من هاليد الألكيل الثانوي أو الثالثي يخضع لحادثة الإنتزاع (E2) بدلاً من الإستبدال النيكليوفيلي (SN2).
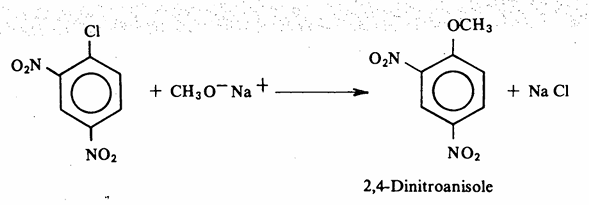
ولا يمكن استخدام هاليدات الأريل في هذا التفاعل نظراً لخمولها الكيميائي تجاه الإستبدال النيكلوفيلي، إلا أنه يمكن استخدام هاليد أريل به مجموعات مثبطة على الحلقة الأروماتية الأمر الذي يزيد من فعالية ذرة الهالوجين في هذا المركب ، على سبيل المثال:



|
|
|
|
مقاومة الأنسولين.. أعراض خفية ومضاعفات خطيرة
|
|
|
|
|
|
|
أمل جديد في علاج ألزهايمر.. اكتشاف إنزيم جديد يساهم في التدهور المعرفي ؟
|
|
|
|
|
|
|
العتبة العباسية المقدسة تقيم ندوة علمية عن روايات كتاب نهج البلاغة
|
|
|