


 علم الكيمياء
علم الكيمياء 
 الكيمياء التحليلية
الكيمياء التحليلية 
 الكيمياء الحياتية
الكيمياء الحياتية 
 الكيمياء العضوية
الكيمياء العضوية 
 الكيمياء الفيزيائية
الكيمياء الفيزيائية
 الكيمياء اللاعضوية
الكيمياء اللاعضوية 
 مواضيع اخرى في الكيمياء
مواضيع اخرى في الكيمياء
 الكيمياء الصناعية
الكيمياء الصناعية |
أقرأ أيضاً
التاريخ: 8-9-2019
التاريخ: 15-10-2020
التاريخ: 10-10-2019
التاريخ: 15-10-2020
|
الأكسدة: تتأكسد الألدهيدات بسهولة وتتحول إلى الحموض الكربوكسيلية المطابقة في حين أن الكيتونات لا تتأكسد تحت نفس الظروف التي تتم عندها أكسدة الألدهيدات. ومن المواد المؤكسدة التي تستخدم لهذا الغرض البرمنجنات والكرومات وفوق الأكاسيد مثل فوق أكسيد الهيدروجين أو فوق أكسيد حمض الخل.
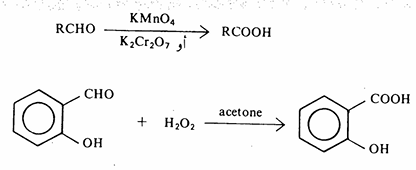
ونظراً لسهولة أكسدة الألدهيدات فإنه يمكن أكسدتها في وجود مواد مؤكسدة أضعف قوة من المواد المؤكسدة سابقة الذكر مثل كاشف تولن (محلول الفضة النشادري( 2(NH3)Ag حيث يختزل أيون الفضة إلى الفضة المعدنية.
الاختزال: سبق وأن أشرنا أن الألدهيدات والكيتونات يمكن اختزالها إلى (ب) الكحولات الأولية والثانوية على التوالي. وقد يتم الاختزال بوساطة الهيدروجين في وجود عامل مساعد البلاتين) أو البلاديوم أو النيكل أو بوساطة مواد كيميائية مختزلة مثل 4LiAIH للعامل المساعد أهميته في عملية الاختزال فإنه بالإمكان اختزال نوع معين من الروابط دون تأثر النوع الآخر عند وجود النوعين القابلة للاختزال معاً في الجزىء وذلك تبعاً لتغير العامل المساعد المستخدم، على سبيل المثال:
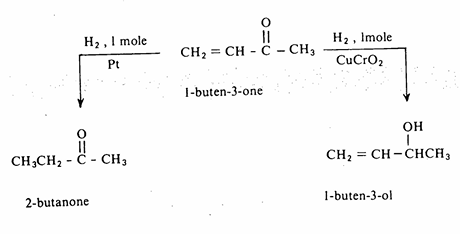
يستخدم الكثير من المواد الكيميائية لاختزال مجموعة الكربونيل
ولكن أكثر هذه المواد استخداما في المختبرات هما LiAIH4 و NaBH4.

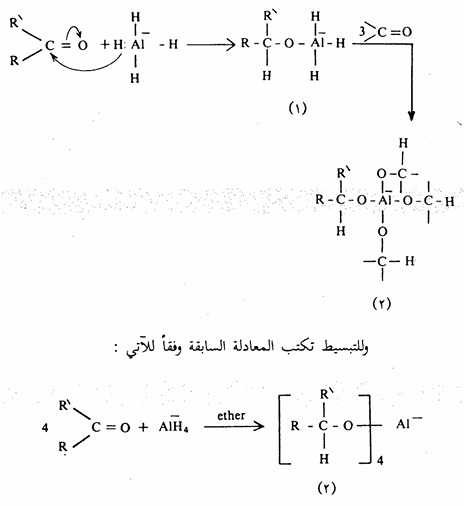
وتمثل كل من مادة LiAIH4 ومادة NaBH4 مصدراً لأيون الهيدريد (H) الذي يهاجم ذرة كربون مجموعة الكربونيل (تفاعل إضافة نيكلوفيلية) لينتج ناتج الإضافة (1) الذي لا يزال في حد ذاته يحوي ثلاث أيونات هيدريد مرتبطة بذرة الألومنيوم وعليه فإن الأمر يحتاج إلى 3 مولات أخرى من المركب الكربونيلي ليتكون ناتج الإضافة (2)، بمعنى آخر تتفاعل أربعة مولات من المركب الكربونيلي مع مول واحد من.LiAlH4
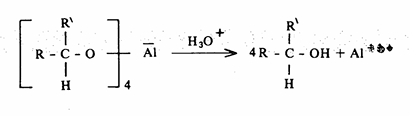
هذا ويتم في خطوة أخرى إضافة الماء المحمض الذي يقوم بدوره بتكسير الروابط الأكسجين والألومنيوم وكذلك إضافة البروتون إلى الأكسجين كي ينتج المركب الكحولي.
ومما تجدر الإشارة إليه أن تفاعلات الاختزال بواسطة LiAIH4 يجب أن تتم في خطوتين منفصلتين تماماً:
أولاً: تفاعل المركب الكربونيلي مع LiAIH4 وتحت ظروف جافة تماماً - في الغالب يستخدم الايثر أو داي جليم Diglyme .
ثانياً: التحلل بواسطة الماء (التميؤ). فمن الضروري بمكان فصل الخطوتين عن بعض نظراً للفعالية الشديدة التي تتمتع بها LiAIHA4 مع المذيبات التي تمثل مصدراً للبروتونات مثل الماء أو الكحول.
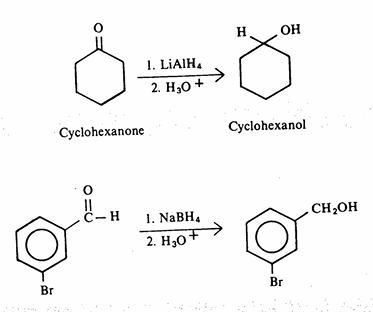
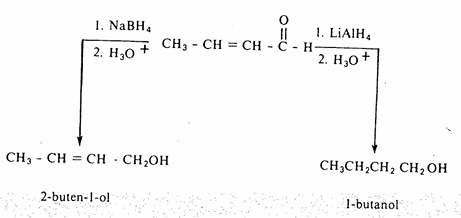
ومن ناحية أخرى فإن NaBH4 تتفاعل ببطء مع الماء أو الكحول وعليه في الكثير من تفاعلات الاختزال بواسطة هذه المادة يستخدم أو الكحول كمذيب وقلة فعالية NaBH4 مقارنة بمادة LiAIH4 تجعل منها ميزة في اختزال مجموعة فعالة وعدم تأثر أخرى إذا ما وجدت هذه المجاميع في نفس الجزىء، على سبيل المثال:
كما ويمكن أن تتحول مجموعة كربونيل الألدهيدات والكيتونات إلى مجموعة مثيلين CH2-- ويتم ذلك بطريقتين سبق ذكرهما هما طريقة كلمنسن وطريقة وولف كيشنر. وناتج الاختزال واحد في الطريقتين بيد أن الاختلاف بينهما يكمن في الكواشف المستخدمة والوسط حيث تتم طريقة كلمنسن في الوسط الحمضي (وعليه تستخدم في اختزال المركبات التي تتأثر بالقواعد في حين تتم طريقة وولف في الأوساط القلوية. وتستخدم هاتان الطريقتان على نطاق واسع التحضير الأرينات ) ألكيلات البنزين( وكبديل لألكلة فريدل ـ كرافتس
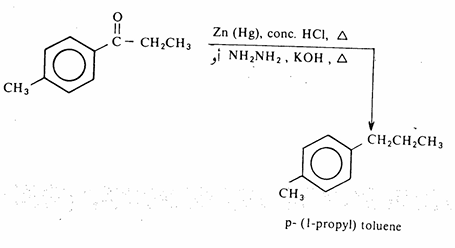
فإذا ما أريد تحضير الكيل بنزين مثل بارا (1 - بروبيل) تولوئین من الألكلة المباشرة للبنزين فإن الناتج يكون خليطاً من الكيلات البنزين.



|
|
|
|
لشعر لامع وكثيف وصحي.. وصفة تكشف "سرا آسيويا" قديما
|
|
|
|
|
|
|
كيفية الحفاظ على فرامل السيارة لضمان الأمان المثالي
|
|
|
|
|
|
|
العتبة العباسية المقدسة تجري القرعة الخاصة بأداء مناسك الحج لمنتسبيها
|
|
|