


 علم الكيمياء
علم الكيمياء 
 الكيمياء التحليلية
الكيمياء التحليلية 
 الكيمياء الحياتية
الكيمياء الحياتية 
 الكيمياء العضوية
الكيمياء العضوية 
 الكيمياء الفيزيائية
الكيمياء الفيزيائية
 الكيمياء اللاعضوية
الكيمياء اللاعضوية 
 مواضيع اخرى في الكيمياء
مواضيع اخرى في الكيمياء
 الكيمياء الصناعية
الكيمياء الصناعية |
أقرأ أيضاً
التاريخ: 2024-01-31
التاريخ: 2024-07-30
التاريخ: 2-10-2016
التاريخ: 2024-06-12
|
الأستيلين acetylene :
الاستخدامات والاقتصاديات : يستخدم الأستيلين مع الأكسجين لإنتاج حرارة عالية للتلحيم وفي تصنيع المواد الكيميائية الصناعية مثل كلوريد الفينيل ، والأكريلونتريل acrylonitrile ، والبولي فينيل بيروليدون polyvinylpyrrolidone ، وثلاثي كلور الإيثيلين trichloroethylene ، وتصنع على الأغلب مادة كيميائية واحدة فقط من الأسيتيلين : الكلوربرين chloroprene وبلمرة النيوبرين polymer neoprene . إن دراسات الضغوط العالية (تقنية ريب Reppe ذات الضغط العالي) مهمة جداً في كون تفاعلات الفنيلة vinylation ، والأثنلة ethynylation، والبلمرة polymerization قد هيأت حقلاً جديداً للكيمياء بإدخالها كثيراً من المركبات الجديدة .
التصنيع : يجري حتى الآن تصنيع الأسيتيلين عن طريق تفاعل كربيد الكلسيوم مع الماء :
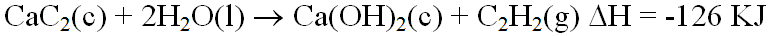
وهناك طريقتان رئيسيتان لتوليد الأسيتيلين من كربيد الكلسيوم . الطريقة المتقطعة وتجري بإضافة الكربيد الى الماء في صهريج أسطواني مائي يعلوه مقر مزود بقادوس ووسائل تغذية . يلقم الكربيد الى الماء بمعدلات محددة حتى يستنفذ . ويفرغ هيدروكسيد الكلسيوم على شكل روبة جير تحتوي على 90 % من الماء تقريبا . اما في الاستخدامات الصناعية الواسعة النطاق فيشيع استخدام المعالجة المستمرة ( الانتاج الجاف ) التي تتميز بالتغذية الآلية . حيث يستخدم 1 كغ من الماء لكل (كغ من الكربيد ، فيتبدد كثير من حرارة التفاعل ( 6.2 M J في القدم المكعب من الاسيتيلين ) عن طرين تبخر الماء ، مخلفا الجير كناتج ثانوي في حالة جافة تسهل جدا معالجته . يمكن تدوير جزء من هذا الناتج الى افران الكربيد . استمرار التحريك ضروري لمنع زيادة التسخين ، لان درجة الحرارة يجب ان تبقى دون 150 مئوية والضغط اقل من 204 KPa .
واحدث الطرق لتصنيع الاسيتيلين هي طريقة تحليل الغاز الطبيعي او الهيدروكربونات السائلة حراريا او تكسيره . وتتضمن المعالجات الاكثر اهمية الاكسدة الجزئية ، واستخدام الاكسجين ، والتكسير الحراري ، والقوس الكهربائي لتامين درجة الحرارة العالية والطاقة . استخدمت طريقة القوس الكهربائي تجاريا في بعض البلدان كألمانيا . تنخفض الطاقة الحرة للاستيلين عند ارتفاع درجات الحرارة . ويكون عند 1600 K ( ١327 مئوية ) واعلى اكثر استقرارا من الهيدروكربونات الاخرى لكنه يتحلل الى عناصر . ولهذا السبب يجب ان يكون زمن التحويل ، او الانشطار قصيرا جدا بشكل لا يصدق ( اجزاء من الف من الثانية) . كمية الطاقة اللازمة كبيرة جدا وفي منطقة الطاقة الحرة المواتية ولكن تحلل CH4 الى عناصر يبدا عند 850 K ( 578 مئوية ) ، وبالتالي يتنافس مع تحلله الى الاسيتيلين . وللتخفيف من هذا التحلل بعد رفع CH4 ( او هيدروكربون اخر ) الى درجة حرارة عالية ، 1500 مئوية ، على مدى اجزاء من مليون من الثانية ، يجب رش كتلا التفاعل بالماء في الوقت نفسه تقريبا.
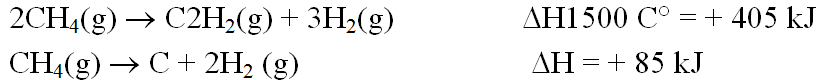
ربما يكون الاحتراق الجزئي للغاز الطبيعي هي الطريقة الاكثر استخداما من قبل خبراء التصنيع الكيميائي . وتظهر هذه الطريقة في الصورة 1 - 1 على شكل مخطط انتاج يتضمن التحويلات الكيميائية الواردة انفا . ويمكن تجزئة المعالجة الى الخطوات المتناسقة التالية :
- يسخن مسبقا وكل على حدة الاكسجين (90 - 98% ) والغاز الطبيعي الى 650 مئوية تقريبا باستخدام غاز الوقود .
- يوجه الغازان ساخنين الى موقد او محول ويمزجان به بنسبة جزيئية غرامية 100 : 0.60 فيما يخص الاكسجين - ميثان .
- يتألف فرن او موقد الاحتراق الجزئي من اجزاء ثلاثة : حجرة المزج ، منطقة الاشتعال ، تليها حجرة الاسقاء بزيت التسقية او مرشات الماء . والتحويل الكيميائي هو احتراق الميتان الجزئي ( الثلثين ) الفوري تقريبا .

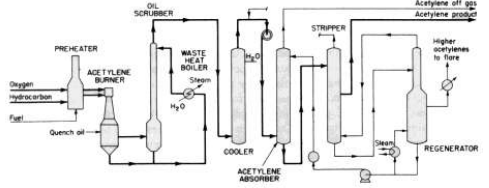
الصورة 1 - 1. مخطة انتاج الاسيتيلين بالأكسدة الجزئية من خامة للهيدروكربونات
- اجمالي تفاعل الميثان ( الاحتراق والانشطار ) هو 90- 95 % ، بينما يتحول الاكسجين بنسبة 100 % . يصل زمن البقاء الى 0.001- 0.01 ثانية .
يتم تبريد الاسيتيلين والغازات بسرعة بزيت السقاية او بمرشات الماء الى مئوية ويكون ترتيبها كما يلي ، % :
|
اسيتيلين |
8.5 |
ميثان |
4 |
|
هيدروجين |
57 |
اسيتيلين عالي |
0.5 |
|
اول اكسيد الكربون |
25.3 |
خاملة |
0.1 |
|
ثاني اكسيد الكربون |
3.7 |
اجمالي |
100 |
- يزال السخام بمرشحة الكربون .
- تضغط الغازات النظيفة الى 1.14 Mpa .
- يزال الاسيتيلين في عمود (محشو) بمذيب انتقائي ، ثنائي مثيل فورم اميد
مثلا . يومض ط ، flashed ثاني اكسيد الكربون ويفصل في الاعلى overhead من
213
المذيب الغني في العود ( المحشو ) ، حيث يجزأ الاسيتيلين ، ليعطي ناتجا +99% بمردود 30-36 % من الكربون في الغاز الطبيعي .
- تفصل الاسيتيلينات العليا والماء عند ضغط منخفض ، وبعاد استخدام المذيب .
تستخدم معالجة والف wulff لإنتاج الاسيتيلين فربا قوميا لتحليل الهيدروكربونات الى اسيتيلين . وقد ثبت انه عالي الكلفة بالنسبة للتنافس مع تكاليف الطاقة التي ارتفعت كثيرا هذه الايام .
يسترجع الاسيتيلين ايضا من خامة اثيلين التغذية قبل بلمرة الاثيلين .



|
|
|
|
لشعر لامع وكثيف وصحي.. وصفة تكشف "سرا آسيويا" قديما
|
|
|
|
|
|
|
كيفية الحفاظ على فرامل السيارة لضمان الأمان المثالي
|
|
|
|
|
|
|
العتبة العباسية المقدسة تجري القرعة الخاصة بأداء مناسك الحج لمنتسبيها
|
|
|