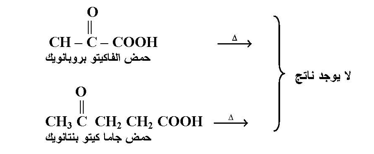
تحتوي مجموعة الكربوكسيل على مجموعة كربونيل ومجموعة هيدروكسيل ، وتتأثر احدهما بالأخرى . فتفاعلات الأحماض الكربوكسيلية مع المحاليل المائية لهيدروكسيد الصوديوم وبيكربونات الصوديوم تكون كما يلي :
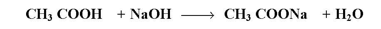
أما عند تفاعل الأحماض الكربوكسيلية بانشطار وإزاحة مجموعة الهيدروكسيل فيتضمن هجوم نيوكليوفيلي يتبعه تقاعل حذف ( أي انها تفاعلات إبدال ) بينما تكون في الالدهيدات والكيتونات تفاعلات إضافة .
التفاعل مع هاليدات الفوسفور والكبريت :
تستخدم عدة كواشف لتحضير كلوريدات الأحماض من الأحماض الكربوكسيلية كما يلي :

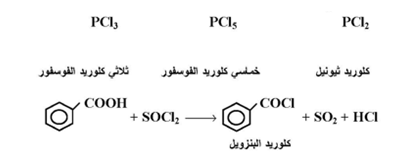
وعادة ما يفضل استخدام كلوريد ثيونيل لسهولة التخلص من النواتج الجانبية الغازية مثل HCl,SO2
تحويل الأحماض الكربوكسيلية إلى اميدات :
تتفاعل الأحماض الكربوكسيلية مع النشادر لتعطي أملاح امونيوم في المرحلة الأولى التي تعطي اميدات عند تسخينها :
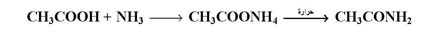
التحول إلى أسترات :
تتفاعل الأحماض الكربوكسيلية مع الكحولات في وجود كمية حفزية من حمض الكبريتيك المركز أو HCl الغازي لتعطي أسترات والأخيرة مركبات لأغلبها روائح محببة وعادة ما نستخدم كنكهات في كثير من أنواع العصير المختلفة .
التفاعل العام :
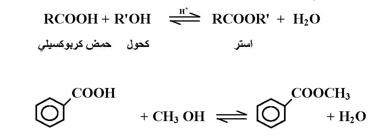
بنزوات ميثيل
ويلاحظ أن الاسترة تفاعل عكسي ولذا ومن أجل دفع الاتزان نحو اليمين فتستخدم كمية وافرة من الكحول أو إزاحة الماء النائج من محيط التفاعل .
التحول إلى انهيدريدات :
يمكن لجزيئي حمض كربوكسيلي عند تسخينها فقد جزيئ ماء ( في وجود خماسي أكسيد الفوسفور ) لتعطي انهيدريد :
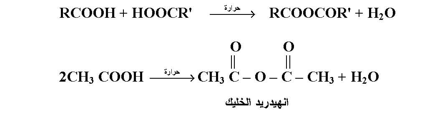
ويمكن الحصول على انهيدريد متماثل أو غير متماثل اعتماداً على الحمض أو الأحماض المستخدمة .
اختزال الأحماض الكربوكسيلية :
تختزل الأحماض الكربوكسيلية وتتحول إلى الكحولات الأولية المقابلة باستخدام هيدريد ليثيوم الومنيوم (LiAIH4 ) عند درجة حرارة منخفضة . بعد التميؤ :
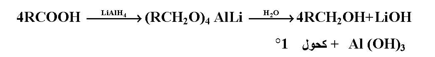
وتعتبر هذه الطريقة من أفضل الطرق لاختزل الأحماض الكربوكسيلية إلى كحولات أولية .
هلجنة الأحماض الكربوكسيلية :
تتفاعل الأحماض الكربوكسيلية التي تحتوي على ذرات هيدروجين من نوع ألفا مع الكلور أو البروم في وجود بعض العوامل الحفازة مثل الفوسفور لتعطي أحماض هالوجينية .
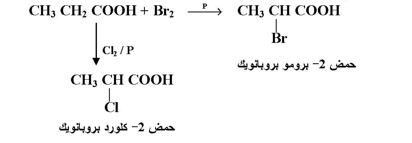
يسمى هذا بتفاعل فولهارد . ويستفاد مثل هذا التفاعل في تحويل أحماض ألفا الهالوجينية إلى مشتقات أخرى بتفاعلها مع الامونيا وهيدروكسيد الصوديوم أو سيانيد الصوديوم :
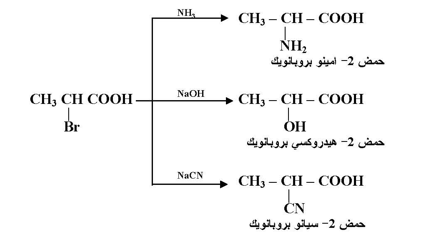
وقد يستمر تفاعل الهالوجين مع حمض كربوكسيلي حتى يتم استنفاد جميع ذرات هيدروجين ألفا :
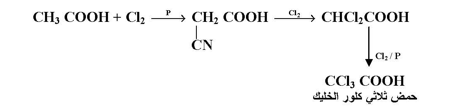
أما الأحماض التي لا تحتوي على ذرات هيدروجين من نوع ألفا فلا تتفاعل مع الهالوجينات عند الظروف المذكورة .
إزالة مجموعة الكربوكسيل :
يتم انتزاع أو إزالة مجموعة الكربوكسيل من أملاح الأحماض الكربوكسيلية عند صهرها مع جير الصودا لتعطي الالكان المقابل بذرة كربون أقل كما يلي :
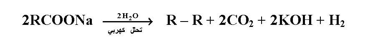
التحليل الكهربي ( تفاعل كولب ) :
تتحل أملاح الأحماض الكربوكسيلية تحللاً كهربياً لتعطي الكانات بنفس الهيكل الكربوني أو هيكل أكبر .

ازالة مجموعة الهيدروكسيل :
يمكن للأحماض الكربوكسيلية التي لديها مجموعة كربونيل بيتا عند تسخينها أن تفقد CO2 من مجموعة الكربوكسيل :
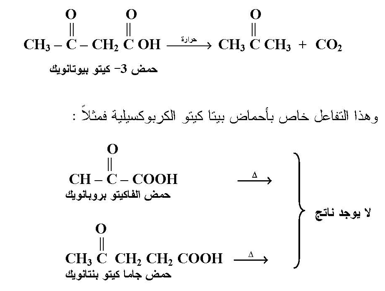
وهذا التفاعل خاص بأحماض بيتا كيتو الكربوكسيلية فمثلاً :