


 علم الكيمياء
علم الكيمياء 
 الكيمياء التحليلية
الكيمياء التحليلية 
 الكيمياء الحياتية
الكيمياء الحياتية 
 الكيمياء العضوية
الكيمياء العضوية 
 الكيمياء الفيزيائية
الكيمياء الفيزيائية
 الكيمياء اللاعضوية
الكيمياء اللاعضوية 
 مواضيع اخرى في الكيمياء
مواضيع اخرى في الكيمياء
 الكيمياء الصناعية
الكيمياء الصناعية | تقنية النانو في وظائف الأعضاء العصبية (الدماغ) Nanotechnology in the functions of nervous organs (the brain) |
|
|
|
أقرأ أيضاً
التاريخ: 2025-02-17
التاريخ: 2025-02-18
التاريخ: 2025-02-18
التاريخ: 2025-02-25
|
يعتبر الكثيرون أن الدماغ هو النظام البيولوجي الأكثر تعقيدًا في الوجود، لذلك ليس من المستغرب أن تدفع المتطلبات التقنية لأبحاث علم الأعصاب الابتكار في العديد من المجالات. شهد العقد الماضي انفجارًا في الأساليب البصرية الجديدة لتسجيل وتحفيز دوائر الدماغ، لا سيما في مجال علم البصريات الوراثي. وبنفس القدر من الأهمية، فإن الأدوات التجريبية والتحليلية الجديدة للفحص المجهري الإلكتروني تتيح الآن إعادة بناء حجمية عالية الدقة للأنسجة العصبية متبوعة بتحليل التوصيل الكمي. وبالنظر إلى التقدم المحرز في هذه المجالات، فمن المدهش أن التسجيل الكهربائي المباشر من الخلايا العصبية - تم النظر فيه منذ فترة طويلة مركزية في أبحاث علم الأعصاب - لم يتغير كثيرًا في العقود الثلاثة الماضية. لا يزال تسجيل رقعة الخلية الكاملة ، وتسجيل مسرى مكروي حاد ، والأقطاب خارج الخلية القائمة على السيليكون هي أحدث ما توصلت إليه التسجيلات العصبية على الرغم من قيودها المعروفة: يتسبب تسجيل رقعة الخلية في غسيل الكلى على مدى دقائق ، وتغير الأقطاب الدقيقة الحادة مقاومة المدخلات وإمكانات غشاء الراحة ، ولا يمكن للتسجيل خارج الخلية أن يقيس التغيرات تحت العتبة في إمكانات الغشاء العصبي الدافع لتطوير أدوات نانوية لعلم وظائف الأعضاء العصبية هو تسجيل النشاط الكهربائي داخل الخلايا من آلاف الخلايا العصبية في وقت واحد دون الإخلال بخصائصها الفسيولوجية. علاوة على ذلك، لجعل هذه الأدوات مؤثرة في علم الأعصاب، يجب أن تكون قوية وسهلة الاستخدام ويمكن إعادة إنتاج أدائها عبر المختبرات أثبتت عدة مجموعات الآن أن الأجهزة النانوية ذات الحالة الصلبة يمكنها تسجيل النشاط الكهربائي في الخلايا العصبية وخلايا عضلة القلب، مما يشير إلى خطوة مهمة نحو التسجيل داخل الخلايا غير متواز وغير ديالي. يتمثل التحدي المتبقي في إثبات إمكانية استخدام هذه الأجهزة على فترات زمنية ذات صلة بالتجارب الفيزيولوجية العصبية مع الحفاظ على الوظيفة الخلوية الأصلية. في الأقسام التالية سوف ندرس القدرات التقنية لإنتاج أجهزة، نانوية والخصائص الكهربائية الذاتية لهذه الأجهزة، وتفاعلها المحدد مع الخلايا. نستنتج أن التفاعل بين الخلية والإلكترود (قطب كهربائي) هو الجانب الأكثر أهمية في تصميم الجيل القادم من الأقطاب الكهربائية داخل الخلايا. سيكون العديد من علماء الأعصاب على دراية بالتطورات المثيرة في مجال الإلكترونيات الحيوية، ويرجع الفضل في ذلك جزئيا إلى العديد من المراجعات الحالية حول هذا الموضوع، حيث تم استخدام الأجهزة النانوية التي تتضمن أسلاكًا نانوية وترانزستورات نانوية لتسجيل النشاط الكهربائي من الخلايا العصبية وخلايا عضلة القلب, يعتمد هذا المجال على مجموعة واسعة من تقنيات التصنيع الحديثة، مما يعني أن بناء ومعالجة الأجهزة على مقاييس الطول دون الخلوية (500 نانومتر) أصبح أمرًا روتينيا الآن، مع بعض الأجهزة التي يتم نقشها على مقياس الطول الفردي. البروتينات. النقش باستخدام الطباعة الحجرية لشعاع الإلكترون بأحجام ميزة 10 نانومتر يكون مستقيما نسبيًا، إذا كان باهظ الثمن، في حين أن الأنماط عند 250 نانومتر وما فوق يمكن الوصول إليها بسهولة باستخدام الطباعة الحجرية الضوئية. وهناك العديد من التقنيات المتاحة لإنتاج أسلاك نانوية قطرها أقل من 100 نانومتر وحتى عشرات الميكرومترات بطول، إما عن طريق الزخرفة والحفر أو ترسيب البخار الكيميائي (CVD) يمكن التحكم في سماكة الأغشية الرقيقة إلى أقل من 1 نانومتر على ركائز مستوية، ومع ظهور ترسيب الطبقة الذرية (ALD) ، يمكن طلاء أكسيد وأغشية معدنية بشكل مطابق على هياكل معقدة وذات نسبة أبعاد عالية ببراعة مماثلة يتم أيضا صنع قشور نانوية بسماكة جدار تتراوح بين 5 و50 نانومتر وأقطار من عشرات إلى آلاف نانومتر بسهولة باستخدام ALD ويمكنها فصل جزء اختراق الغشاء لجهاز التسجيل عن جزء الاستشعار الكهربائي. طريقة سهلة أخرى للبنى النانوية الموصلة هي النمو الكهروكيميائي المقولب، والذي يمكن أن ينتج الأنابيب النانوية والقضبان النانوية، والأعمدة الدقيقة، بما في ذلك الهياكل النطاقات ذات التركيب غير المتجانس. كما تم تصنيع ترانزستورات تأثير المجال النانوي للتسجيلات الخلوية بعضها بالاشتراك مع تصاميم نانوسترو أخيرًا، تم استخدام تقنيات الأغشية الرقيقة والطبقات الأحادية المجمعة ذاتيًا لإنشاء عصابات كارهة للماء من 3 إلى 5 نانومتر على جوانب الهياكل النانوية غير العضوية، مما يسمح لها بالاندماج في بروتينات الغشاء ثنائية الطبقة الدهنية. باختصار، فإن صندوق أدوات النانو قادر على إنتاج أي تصميم تقريبًا إلى مستوى 10 نانومتر، مما يجعل السؤال المركزي ليس كيفية البناء، ولكن ما الذي يجب بناؤه. ان ميزة النانو الحجة الأكثر وضوحًا لاستخدام أجهزة التسجيل المصنعة بالنانو هي الحجة ذات الحجم الكبير: يمكن للأقطاب الكهربائية الأصغر أن تسجل من بنى أصغر وتكون معبأة بكثافة أكبر للتسجيل من خلايا أكثر مع إزاحة أقل للحجم في الجسم الحي. وبالتالي، إذا كانت جميع الأشياء الأخرى متساوية، فإن الأجهزة الأصغر تكون أفضل لرسم خرائط النشاط المتوازي على نطاق واسع. ثانيًا، لوحظ على نطاق واسع أن الخلايا " تلتف " تلقائيًا، أو تبتلع الهياكل النانوية البارزة، وهذا الاتصال الحميم بين الخلية والإلكترود يبسط إسناد مصدر الإشارة قطب كهربائي واحد، وخلايا عصبية واحدة) ويحسن نسبة الإشارة إلى الضوضاء مقارنة بالتسجيل المستوي الأنظمة مصفوفات مسرى النانو الموصوفة في الأدبيات الحديثة ليست مجرد مصفوفات أقطاب ميكروية أصغر، ولكنها تتفاعل مع الخلايا بطرق مختلفة نوعيًا. ميزة رئيسية أخرى لاستخدام جهاز تسجيل نانوي الحالة الصلبة هي أنه يمكن استخدامه داخل الخلايا دون الإخلال بتكوين السيتوبلازم يؤدي التخلص من موصل الإلكتروليت السائل المستخدم في الأساليب القائمة على الماصة المجهرية إلى حل فوري لمشكلة الانتشار بين الخلية ومحلول الماصة، والتي تمثل مشكلة خاصة لتسجيل الخلية الكاملة، ولكن أيضًا للأقطاب الكهربائية الدقيقة باستخدام المحاليل الداخلية عالية القوة الأيونية نظرًا لأن الموصلات المعدنية تتمتع بموصلية أعلى من 107 مرات مقارنة بمحاليل الإلكتروليت النموذجية، فهناك حجة محددة لتقليل مساحة المقطع العرضي للإلكترود عن طريق التحول إلى أجهزة الحالة الصلبة. تم إجراؤها نحو الأتمتة وتقنية تثبيت التصحيح في الجسم الحي، فإن المتطلبات الميكانيكية للتحكم في الضغط أي صلابة الماصة) لا تتناسب مع التسجيلات المتوازية بشكل كبير من ناحية أخرى تم تصميم التصنيع النانوي للتوازي، مما ينتج بشكل روتيني هياكل معقدة بنفس مقاييس الطول مثل المكونات الخلوية (3-30 نانومتر) ، مما يعني أنه يمكن تصميم الأجهزة للتفاعل مع الخلايا على المستوى تحت الخلوي ، كما يسهل الاندماج في الكترونيات القراءة بشكل كبير من خلال العمل مع المجسات الإلكترونية ذات الحالة الصلبة ، ويمكن ربط مصفوفات الهياكل النانوية بواسطة رقاقة فليب. طرق إلكترونيات CMOS عالية الكثافة للتسجيل والتحفيز. التسجيل الكهربائي من الأجهزة النانوية هناك عدة طرق متميزة للتسجيل الكهربائي بمقياس نانوي. لإظهار اتساع الأحجام والأشكال، تتم مقارنة الصور الظلية لبعض الأجهزة التمثيلية في الشكل (5.3) جنبا إلى جنب مع ماصة التصحيح والإلكترود الدقيق الحاد. الأجهزة الموضحة في الصف السفلي من الشكل (6.3) متصلة بركيزة مسطحة وتتفاعل مع الخلايا المستنبتة التي إما نمت على ركائز أو يتم تسليمها إليها الأجهزة الموضحة في الصف العلوي من الشكل 1 عبارة عن أجهزة مدخلة، يتم توصيلها بواسطة معالج دقيق إلى الخلية، حيث يخترق جزء التسجيل غشاء البلازما لتحقيق الوصول إلى العصارة الخلوية. يقارن الشكل (7.3) العديد من التسجيلات الكهربائية باستخدام أجهزة نانوية حيث تم قياس إمكانات الغشاء بشكل مستقل إما بواسطة ماصة التصحيح أو مسرى دقيق حاد لقد حفزت هذه النجاحات المبكرة قدرًا كبيرًا من الاهتمام لتوسيع تصميمات مسرى النانو إلى مصفوفات أجهزة متوازية على نطاق واسع في الجسم الحي من وجهة نظر التسجيل الكهربائي، فإن أهم تمييز بين أجهزة التسجيل النانوية هذه هو ما إذا كانت تخترق غشاء الخلية أم لا. يحدد هذا ما إذا كان القطب سيقيس مباشرة إمكانات الغشاء )الشكل (A5أو ما إذا كان سيقيس الإمكانات المحلية خارج الخلية (الشكل 5 B-D). إذا كان القطب النانوي مجاوزا للخلية فقط، فإنه يتصرف كما لو كان MEA تقليديا (الشكل5B)، يقيس شكل موجة محتمل للعمل خارج الخلية ولا توجد إشارة تقريبا من تغييرات العتبة الفرعية في الإمكانات. عندما ينتج عن ابتلاع القطب النانوي ختم فضفاض بين الغشاء والقطب الكهربي، يلاحظ أيضا شكل موجة خارج الخلية الكنسي الشكل 5C، ولكن عندما يكون الختم محكما للغاية، قد يحاكي الجيب المغلف للحل عن كتب الإمكانات داخل الخلايا وستكون المكونات منخفضة التردد لإمكانات العمل مرئية الشكل ثلاثي الأبعاد. في الواقع، قد تكون تفاعلات الإلكترود النانوي مع الخلية معقدة مع اختراق جهاز جزئيًا للغشاء وابتلاعه جزئيًا، ولكن من أجل الوضوح ولإدخال أهم الخصائص الكهربائية للتكوينات المختلفة، وصفنا هنا بشكل منفصل اثنين من التكوينات العامة للتسجيل: أقطاب اختراق الخلايا وأقطاب سيلنغولفيد.
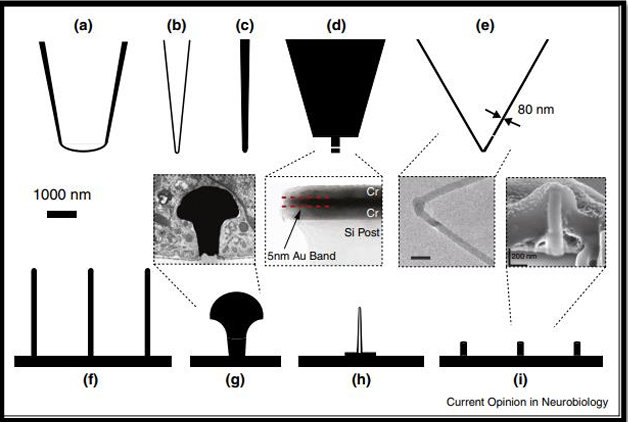
الشكل (5.3) حجم وشكل الأجهزة النانوية
يتم عرض الأجهزة النانوية المختلفة لتوسيع نطاق المقارنة مع بعضها البعض ومع الأجهزة التقليدية طرق التسجيل داخل الخلايا (a) ماصة التصحيح التقليدية؛ (b) مسرى دقيق حاد؛ (c) القطب النانوي (d) مسبار التخفي (e) الترانزستور النانوي (f) مصفوفة الإلكترود النانوي (8) القطب الصغري (h) الأنبوب النانوي - جهاز الترانزستور النانوي و (i) قطب الأنبوب النانوي
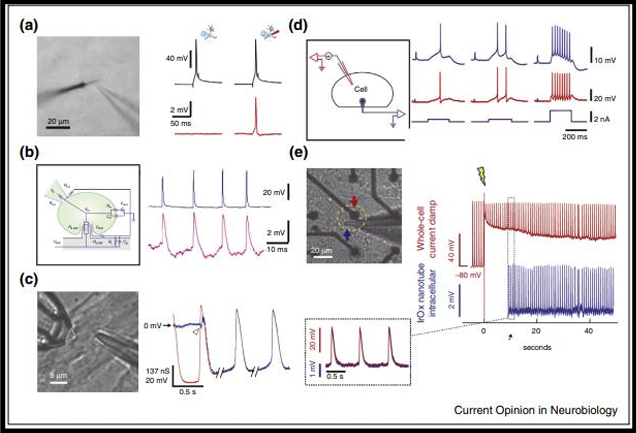
الشكل (6.3) تسجيل الخلايا العصبية.
قدرات التسجيل الكهربائي للأجهزة النانوية تم اختيار هذه التسجيلات على وجه الخصوص لأنها أجريت جنبًا إلى جنب مع تسجيلات التحكم المتزامنة إما بواسطة ماصات التصحيح أو أقطاب كهربائية دقيقة(a) التسجيل داخل الخلايا من الخلايا العصبية الهرمية في شريحة الحصين العضوية، باستخدام قطب كهربائي نانوي من التنغستن هنا يتم تسجيل شكل موجة محتمل للعمل بواسطة مشبك التصحيح للخلية الكاملة (أسود) قبل وبعد اختراق مسرى النانو (يحدث خلال فترة 30 مللي ثانية بين الآثار)؛ (b) التسجيل من الخلايا العصبية المزروعة التي تنمو على مصفوفة مسرى نانوي من أسلاك السيليكون النانوية المطلية بالذهب. ينتج عن الحقن الحالي بواسطة ماصة التصحيح (الزرقاء) إمكانات العمل التي يمكن قياسها أيضا على مسرى النانو (الوردي) (c) التسجيل داخل الخلايا من خلية عضلية القلب باستخدام ترانزستور تأثير المجال النانوي (FET) هنا يغير الجهد الكهربائي عند طرف المسبار مباشرة ناقل FET (أزرق) يمكن تراكب شكل الموجة التحويلية هذا مع تسجيل رقعة الخلية الكاملة المتزامن (أحمر) ويكشف عن مدى دقة تتبع FET لإمكانات الغشاء. ويتضح أيضا من تسجيل التحكم عند إدخال FET في الغشاء، لوحظ تغيير في إمكانات غشاء الراحة؛ (d) تسجيلات الخلية، على الرغم من أن خارج الخلية (الأزرق) تتبع إمكانات الغشاء لعصب Aplysia مع دقة ملحوظة، كما هو موضح من خلال تسجيل مسری دقيق متزامن حاد (جهد أحمر، تيار محقون أرجواني)؛ و (e) يمكن إجراء التسجيلات الكهربائية التي تدوم لعشرات الدقائق بشكل دوري على الخلايا العضلية القلبية المزروعة على مدى أيام باستخدام مصفوفات الأنابيب النانوية من أكسيد الإيريديوم للحصول على وصول عابر داخل الخلايا، تم دفع قطب الأنبوب النانوي بجهد عالي لكهرباء الغشاء (0 = t) أدى ذلك إلى تغيير إمكانات غشاء الراحة كما هو موضح من خلال تسجيل التصحيح المتزامن (أحمر) ولكنه أدى أيضًا إلى خصائص تسجيل ممتازة من الأنبوب النانوي (الأزرق) كدليل من خلال تراكب التسجيلين (داخلي).
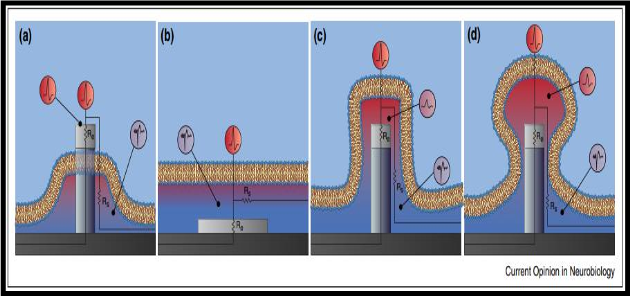
الشكل (7.3) القطب الكهربائي وغشاء الخلية
تكوين القطب الكهربائي والغشاء (a) قطب كهربائي نموذجي مستو خارج الخلية. يكون التفاعل بين القطب الكهربائي والغشاء ضئيلا بشكل عام، وتكون مقاومة الختم منخفضة، وبالتالي يسجل القطب الموجي التقليدي خارج الخلية؛ (b) الوصول المباشر داخل الخلايا؛ (c) التسجيل الغامض السائب بشكل أساسي تسجيل خارج الخلية، ولكن قد تكون سعة السنبلة كبيرة مثل الميليفولت بسبب عزل الجيب المبتلع عن محلول الحمام؛ (d) التسجيل المغمور بإحكام عندما تقترب مقاومة ختم الغشاء والإلكترود من مقاومة الغشاء للرقعة المبتلة، يمكن أن تكون إمكانات الجيب مشابهة جدا للجهد داخل الخلايا، وبالتالي فإن الشكل الموجي المقاس يشبه إلى حد كبير التسجيل داخل الخلايا.



|
|
|
|
النوم 7 ساعات ليلا يساعد في الوقاية من نزلات البرد
|
|
|
|
|
|
|
اكتشاف مذهل.. ثقب أسود ضخم بحجم 36 مليار شمس
|
|
|
|
|
|
|
خلال شهر رمضان.. العتبة العباسية المقدسة تستعد لإقامة أنشطة دينية وثقافية في باكستان
|
|
|