


 النبات
النبات
 الحيوان
الحيوان
 الأحياء المجهرية
الأحياء المجهرية
 علم الأمراض
علم الأمراض
 التقانة الإحيائية
التقانة الإحيائية
 التقنية الحيوية المكروبية
التقنية الحيوية المكروبية
 التقنية الحياتية النانوية
التقنية الحياتية النانوية
 علم الأجنة
علم الأجنة
 الأحياء الجزيئي
الأحياء الجزيئي
 علم وظائف الأعضاء
علم وظائف الأعضاء
 الغدد
الغدد
 المضادات الحيوية
المضادات الحيوية|
أقرأ أيضاً
التاريخ: 2-9-2020
التاريخ: 9-3-2018
التاريخ: 6-7-2017
التاريخ: 14-10-2015
|
مخطط راماجاندران Ramachandran Plot
مخطط يرسم لمكونات البروتينات او الببتيدات لايجاد الوضع الطبيعي لتوزيع الذرات في البروتينات الطبيعية اذ ان تكوين الآصرة الببتيدية يحتاج الى إضافة طاقة حرة، وتكون هذه الآصرة ثابتة جدا. وعندما تكون الآصرة التي تكون في مستوي تحتم على مكونات الحوامض الامينية توزيع يحدد بالزوايا المزدوجة φ Dihedral Angles الواقعة بين النتروجين وكربون ألفا ، والزاوية ψ الواقعة بين ذرة Cα وكربون الكربوكسيل فهذه يمكن ان تختلف وتمثل درجات حرية للبروتين وهي التي تحدد الأبعاد الثلاثية للبروتينات فيما بعد. اذ انها تقييد بقياسات تسمح بتراكيب ثانوية محددة وليست مطلقة ومن ثم يترتب عليه تكوين التراكيب الثانوية وطوي البروتينات وهذه الزوايا موضحة في الشكل الاتي :
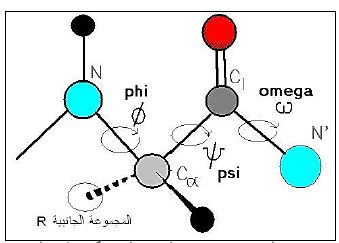
وتتراوح قيم الزوايا بين +180ºالى -180º ، فالدوران باتجاه عقرب الساعة يعطي الزوايا قيم موجبة وبالعكس ولذلك تسمى هذه الزوايا في بعض الأحيان بزوايا الانفتال Torsion Angles .ان توائم الزاويتين ليس مطلقا كما انه في بعض الأحيان لا توجد توافقية نتيجة لتصادم الذرات ، وهذه العلاقات تحدد بمخطط راماجاندران الموضح في الشكل الاتي :
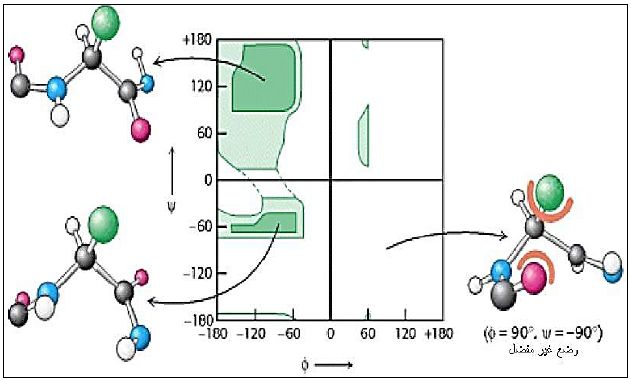
والشكل يوضح قيم الزوايا φ وψ التي يمكن ان توجد بين الذرات فيشير الشكل مثلا الى انه عندما تكون φ قائمة و ψ قائمة بالاتجاه المعاكس (اي قيم سالبة) فهو وضع غير ملائم. ويشير الشكل ايضا الى ان ثلاثة أرباع وحدة الدائرة (وحدة الدائرة بأرباعها الأربعة في القياسات الرياضية) لا تكون ملائمة وان هناك قيم خاصة فقط هي التي تسمح بان يكون توزيع الذرات ملائما كما موضح في اللون الأخضر الغامق والأقل منها تفضيلا والأخضر ألفاتح ، اذ ان القيم العامة تؤدي الى عمليات تصادم بين الذرات وتؤدي الى استبعاد الذرات والتي تكون من الأساسيات المميزة لتوزيع الذرات المجسم وذلك لانه لا يمكن ان تكون ذراته في المكان نفسه وفي الوقت نفسه ، وجزء من هذا التأثير تضفيه السلاسل الجانبية للحوامض الامينية من حيث صفات حجمها او مجاميعها الفعالة او غيرها من الصفات.
وبالعودة الى الحقائق المذكورة سابقا وفحص هيكل البروتين تتضح عدة حقائق منها ان الآصرة الببتيدية هي مستوية بشكل أساس وعليه فعند ارتباط اثنين من الحوامض الامينية فان الست ذرات المكونة لهما ستكون في المستوى نفسه (افتراضا) ، والحقيقة الأخرى ان الآصرة الببتيدية تمتلك بعض صفات الأواصر المزدوجة نتيجة اشتراك الكترونات بين الذرات O=C-N والتي تمنع دوران الذرات حولها وهذا ما يؤدي الى استواء الآصرة اي تكوين مستوى الآصرة Peptide Plane، ونظرا للتركيب الصلد الذي تبديه الآصرة الببتيدية وثبوتيتها فهي تجبر الذرات المرتبطة بها على ان تقع في المستوى نفسه ولكن بتقيدات |(كما ذكر آنفا). وصفة الآصرة المزدوجة التي تمتلكها يعبر عنها بطول الآصرة التي تربط بين CO و NH فطول الآصرة بين C-N هي 1.32 انكستروم في حين ان الآصرة المفردة (العادية) بين C-N تبلغ 1.49 انكستروم اما في حالة وجود الآصرة المزدوجة بين العنصرين C=N فتكون قيمتها 1.27 انكستروم والشكل التالي يوضح أطوال الأواصر :
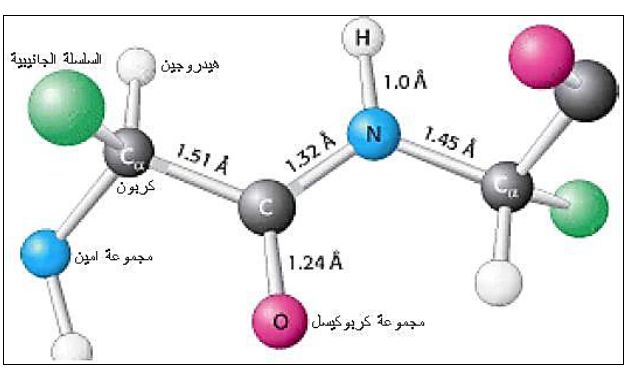
ان الآصرة الببتيدية غير مشحونة وبعد استقرار الذرات وفق قيم الزوايا الازدواجية يمكن ان تنشأ سلاسل من الحوامض الامينية التي يكون فيها توزيع الحوامض الامينية حول محور السلسلة بالشكل المتخالف Trans وفيه تقع ذرتي Cα على جانبي الآصرة الببتيدية، او تكون بالوضع المتوافق Cis وفيه تقع ذرتي Cα للحامضين المتجاورة على الجهة نفسها من مستوى الآصرة الببتيدية .



|
|
|
|
لصحة القلب والأمعاء.. 8 أطعمة لا غنى عنها
|
|
|
|
|
|
|
حل سحري لخلايا البيروفسكايت الشمسية.. يرفع كفاءتها إلى 26%
|
|
|
|
|
|
|
العتبة العباسية تبحث سبل التعاون مع شركة التأمين الوطنية
|
|
|