


 علم الكيمياء
علم الكيمياء 
 الكيمياء التحليلية
الكيمياء التحليلية 
 الكيمياء الحياتية
الكيمياء الحياتية 
 الكيمياء العضوية
الكيمياء العضوية 
 الكيمياء الفيزيائية
الكيمياء الفيزيائية
 الكيمياء اللاعضوية
الكيمياء اللاعضوية 
 مواضيع اخرى في الكيمياء
مواضيع اخرى في الكيمياء
 الكيمياء الصناعية
الكيمياء الصناعية |
أقرأ أيضاً
التاريخ: 2023-06-28
التاريخ: 22-10-2019
التاريخ: 16-5-2017
التاريخ: 9-10-2020
|
تعتبر مركبات البروبان والبيوتان الحلقية ومشتقاتهما ذات نشاط كيميائي ذات طاقة عالية أو بمعنى آخر قليلة الاستقرار بسبب التوتر الزاوي لهذين المركبين ومشتقاتهما. ومنشأ ذلك التوتر هو كون الزاوية بين الروابط في تلك المركبات أقل من زاوية الهرم الرباعي (109.0) كما في الألكانات المفتوحة كما بينه العالم باير في نظريته. ففي البروبان الحلقي الزاوية الداخلية 60ه وذلك لكون الجزىء يأخذ الشكل المثلث. وفي البيوتان الحلقي فإن الزاوية الداخلية 90ه وذلك لكون الجزيء . يأخذ الشكل المربع هذا الانضغاط المفروض على الزاوية في كل من البروبان والبيوتان الحلقي يؤدي إلى إجهاد وعدم ثبات المركب ويسمى بالإجهاد أو التوتر الزاوي.

أما بالنسبة للبنتان الحلقي والهكسان الحلقي ومشتقاتهما فهي نسبيا مركبات ثابتة وذراتهما لا تقع على مستوى ،واحد وذلك بسبب التوتر الزاوي الذي يغير الوضع المستوى إلى وضع غير مستوى أكثر ثباتاً (أقل طاقة).
ففي البنتان الحلقي تكون الزاوية الداخلية ه108، أي قريبة من زاوية الهرم الرباعي (ه109.0) وبذلك يكون الإجهاد الزاوي ضئيلاً. وحتى يقل الاجهاد في البنتان الحلقي فإن أحد ذراته تقع في مستوى مختلف عن الذرات الأربع الأخرى. وذلك حتى تكون بعض ذرات الهيدروجين في وضع متبادل وبالتالي يقل التنافر الحاصل بسبب السحابة الالكترونية الموجودة على ذرات الهيدروجين.
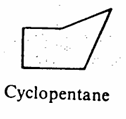
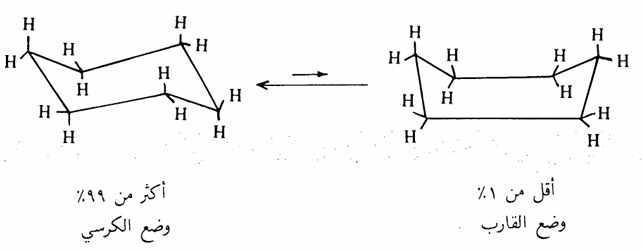
أما جزىء الهكسان الحلقي فلا تقع ذراته في مستوى واحد. وذلك لأن زاويته سوف تكون 120ه لو كانت ذراته في مستوى واحد ولكي تكون زاويته 109.0ه أي زاوية الهرم الرباعي ويخلو من أي إجهاد زاوي ويصل إلى أقصى درجة استقرار فإن ذراته يجب أن لا تقع في مستوى واحد وأن يتخذ أحد وضعين اما الكرسي Chair conformation أو وضع القارب Boat conformation
. وقد وجد وضع الكرسي ووضع القارب في حالة اتزان ولكن وضع الكرسي أكثر ثباتاً بكثير حيث يمثل أكثر من 99٪ من حالة الاتزان، وذلك لأن التنافر الحاصل بسبب ذرات الهيدروجين يكون أقل في حالة وضع الكرسي منه في وضع القارب حيث أن ذرات الهيدروجين تكون في وضع متبادل وليس متقابل.
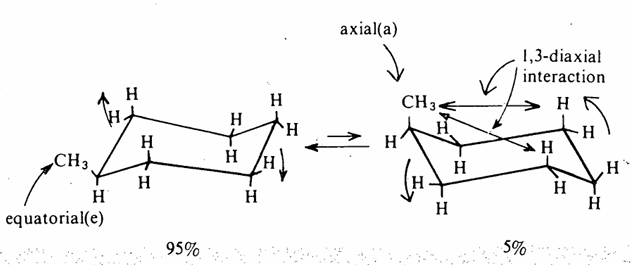
وقد بينت الدراسات التجريبية أن ذرات الهيدروجين في جزىء الهكسان الحلقي في وضع الكرسي يمكن أن تأخذ وضعين. فكل ذرة كربون تحمل ذرتي هيدروجين إحداهما تكون في وضع أفقي والأخرى تكون في وضع رأسي (عمودي) وعندما تستبدل إحدى ذرات الهيدروجين بمجموعة بديلة، فإن هذا البديل إما أن يأخذ وضعاً أفقياً أو رأسياً وقد وجد بالفعل أن الوضعين في حالة اتزان ولكن وجد أيضاً أن الوضع الأفقي دائماً أكثر ثباتاً من الوضع الرأسي وذلك بسبب التنافر الذي يحصل بين السحابة الالكترونية على تلك المجموعة عندما تكون في الوضع الرأسي وبين ذرات الهيدروجين في الوضع الرأسي وهذا ما يعرف بالتنافر بين الوضعين3,1 الرأسيين Diaxial interaction - 1,3



|
|
|
|
لصحة القلب والأمعاء.. 8 أطعمة لا غنى عنها
|
|
|
|
|
|
|
حل سحري لخلايا البيروفسكايت الشمسية.. يرفع كفاءتها إلى 26%
|
|
|
|
|
|
|
المجمع العلمي يحتفي بذكرى ولادة أمير المؤمنين (عليه السلام) في مجمع العلقمي
|
|
|