

علم الكيمياء

تاريخ الكيمياء والعلماء المشاهير

التحاضير والتجارب الكيميائية

المخاطر والوقاية في الكيمياء

اخرى

مقالات متنوعة في علم الكيمياء

كيمياء عامة


الكيمياء التحليلية

مواضيع عامة في الكيمياء التحليلية

التحليل النوعي والكمي

التحليل الآلي (الطيفي)

طرق الفصل والتنقية


الكيمياء الحياتية

مواضيع عامة في الكيمياء الحياتية

الكاربوهيدرات

الاحماض الامينية والبروتينات

الانزيمات

الدهون

الاحماض النووية

الفيتامينات والمرافقات الانزيمية

الهرمونات


الكيمياء العضوية

مواضيع عامة في الكيمياء العضوية

الهايدروكاربونات

المركبات الوسطية وميكانيكيات التفاعلات العضوية

التشخيص العضوي

تجارب وتفاعلات في الكيمياء العضوية


الكيمياء الفيزيائية

مواضيع عامة في الكيمياء الفيزيائية

الكيمياء الحرارية

حركية التفاعلات الكيميائية

الكيمياء الكهربائية


الكيمياء اللاعضوية

مواضيع عامة في الكيمياء اللاعضوية

الجدول الدوري وخواص العناصر

نظريات التآصر الكيميائي

كيمياء العناصر الانتقالية ومركباتها المعقدة


مواضيع اخرى في الكيمياء

كيمياء النانو

الكيمياء السريرية

الكيمياء الطبية والدوائية

كيمياء الاغذية والنواتج الطبيعية

الكيمياء الجنائية


الكيمياء الصناعية

البترو كيمياويات

الكيمياء الخضراء

كيمياء البيئة

كيمياء البوليمرات

مواضيع عامة في الكيمياء الصناعية

الكيمياء الاشعاعية والنووية
ترتب الأنيونوتروبك
المؤلف:
أ. د محمد مجدي واصل
المصدر:
اساسيات الكيمياء العضوية
الجزء والصفحة:
ص 80
2023-07-27
844
يمكن توضيح هذا النوع من الترتبات من خلال ثلاثة خطوات تشمل الخطوة الأولى تكوين الكاتيون الكاربوني في حالة الكاربون أو أيون النايترين في حالة النيتروجين بينما تشمل الخطوة الثانية الترتب الذي تعانيه الجزيئة أما الخطوة الثالثة فتتضمن إعادة هيئة الجزيئة بشكلها المتعادل :
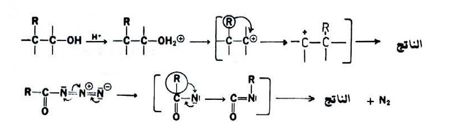
ونجد أن أيون الكاتيون الكاربوني المتكون يكون أكثر شيوعاً وأنه غالباً ما يعاني من الترتب من خلال انتقال إحدى المجاميع العضوية : R ) الخطوة الثانية في المعادلة السابقة ) أو ذرة الهيدروجين (H) بزوجها الالكتروني إلى ذرة الكاربون المجاورة والفقيرة بالالكترونات .
ولما كانت المجموعة المهاجرة هي مجموعة نيكلوفيلية ( OH مثلاً( لذلك فإنها تخضع إلى تحديدات تفاعل التعويض النيكلوفيلي الضمني والتي تشمل على نوعين من التفاعلات : تفاعلات Sn1 تفاعلات Sn2 .
ففي تفاعلات الترتب المشابه إلى Sn2 تساعد المجموعة المهاجرة في المعادلة التالية على دفع المجموعة التاركة ( ϔ ) من خلال تفاعل ذي خطوة واحدة وبصورة مشابهة إلى تفاعلات Sn2 . بينما في تفاعلات الترتب المشابه إلى Sn1 تنظر المجموعة المهاجرة مغادرة المجموعة التاركة لكي تنتقل ( المعادلة التالية(.
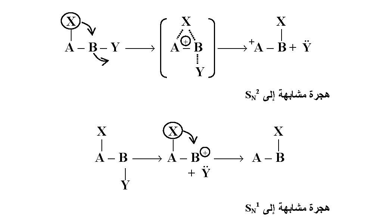
كما وأن هناك حالات أخرى تحمل المجموعة المهاجرة زوجها الالكتروني إلى ذرة الكاربون القريبة منها ( أي أنها تعمل كمجموعة نيكلوفيلية : X في المعادلة التالية ) والحاوية على مجموعة تاركة ( Υ( مكونة وسطاً جسرياً . والذي يكون كاتيوناً عادة .
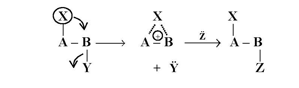
ويمكن أن يتفاعل مع مجموعة نيكلوفيلية أخرى (Z مثلاً : المعادلة السابقة لتكوين الناتج النهائي من خلال رجوع المجموعة ( X ) مع زوجها الالكتروني إلى موقعها الأول ويسمى هذا النوع من المجاميع المؤثرة في طبيعة التفاعل بتأثير المجموعة المجاورة .
ويلاحظ في هذا النوع من التفاعلات بأن سرعة التفاعل تكون أكثر بكثير من السرعة المتوقعة إضافة إلى وجود إعادة في تراتيبها عند مراكزها غير المتناظرة ( الكيرالية ) . بينما لا يلاحظ وجود انقلاب (Inversion ) كما في حالة Sn2
لذلك يوجد في هذا النوع من التفاعلات عادة مجموعة حاوية على زوج الكتروني طليق في الموقع بيتا من المجموعة التاركة . وتسمى الميكانيكية التي يشارك فيها إلى هذا النوع من المجاميع ميكانيكية المجموعة المجاورة .
وعند مراجعة الذرات أو المجاميع الموجودة في بعض المركبات العضوية التي تمتلك هذه الصفة نجد أن هناك عدداً لا بأس به من هذه الذرات أو المجاميع الحاوية أما على زوج الكتروني طليق كما في حالة  والبروم ( Br ) أو حاوية على الكترونات π مثل الأوليفينات والمركبات الأروماتية التي لها القابلية على الانتقال كما يلي :
والبروم ( Br ) أو حاوية على الكترونات π مثل الأوليفينات والمركبات الأروماتية التي لها القابلية على الانتقال كما يلي :
