

علم الكيمياء

تاريخ الكيمياء والعلماء المشاهير

التحاضير والتجارب الكيميائية

المخاطر والوقاية في الكيمياء

اخرى

مقالات متنوعة في علم الكيمياء

كيمياء عامة


الكيمياء التحليلية

مواضيع عامة في الكيمياء التحليلية

التحليل النوعي والكمي

التحليل الآلي (الطيفي)

طرق الفصل والتنقية


الكيمياء الحياتية

مواضيع عامة في الكيمياء الحياتية

الكاربوهيدرات

الاحماض الامينية والبروتينات

الانزيمات

الدهون

الاحماض النووية

الفيتامينات والمرافقات الانزيمية

الهرمونات


الكيمياء العضوية

مواضيع عامة في الكيمياء العضوية

الهايدروكاربونات

المركبات الوسطية وميكانيكيات التفاعلات العضوية

التشخيص العضوي

تجارب وتفاعلات في الكيمياء العضوية


الكيمياء الفيزيائية

مواضيع عامة في الكيمياء الفيزيائية

الكيمياء الحرارية

حركية التفاعلات الكيميائية

الكيمياء الكهربائية


الكيمياء اللاعضوية

مواضيع عامة في الكيمياء اللاعضوية

الجدول الدوري وخواص العناصر

نظريات التآصر الكيميائي

كيمياء العناصر الانتقالية ومركباتها المعقدة


مواضيع اخرى في الكيمياء

كيمياء النانو

الكيمياء السريرية

الكيمياء الطبية والدوائية

كيمياء الاغذية والنواتج الطبيعية

الكيمياء الجنائية


الكيمياء الصناعية

البترو كيمياويات

الكيمياء الخضراء

كيمياء البيئة

كيمياء البوليمرات

مواضيع عامة في الكيمياء الصناعية

الكيمياء الاشعاعية والنووية
تكاثف الالدول
المؤلف:
أ. د محمد مجدي واصل
المصدر:
اساسيات الكيمياء العضوية
الجزء والصفحة:
ص 117 -118 -119-120
2023-07-30
3188
تعاني الالديهيدات والكيتونات الحاوية على ألفا - هيدروجين من تكاثف ذاتي بتأثير قاعدة أو حامض مخففين ، إلا أنه تستخدم في أغلب الحالات قواعد مخففة لتعطي
بيتا - هيدروكسي الديهيد أو بيتا – هيدروكسي كيتون . يسمى هذا النوع من التكاثف تكاثف الدول . وفيما يلي بعض الأمثلة لهذا النوع من التكاثفات كما في :

يتضح من الأمثلة السابقة أن الالديهيدات (اسيتالديهيد وبروبيونالديهيد) والكيتون ( الأسيتون ) والتي عانت من التفاعل احتوت جميعها ذرة ألفا - هيدروجين ؛ وعليه فإن الالديهيدات والكيتونات التي يرغب بتكثفها من خلال تكاثف الدول يجب أن تحتوي على ألفا - هيدروجين شرطاً لحدوث التكاثف .
وفيما يلي بعض من المركبات الكاربونيلية التي لا يمكنها التكاثف ذاتياً تحت شروط تكاثف الدول ( قاعدة مخففة ) لعدم احتوائها على ذرة ألفا - هيدروجين .
البنزالديهيد ، فورمالديهيد ، 2 ، 2 - ثتائي ميثيل بروبيونالديهيد ؛ البنزوفينون والكيتون ثلاثي التعويض ArCOCR .
ويمكن تصور الميكانيكية المقبولة لهذا التفاعل ( والمحفز بقاعدة مخففة ) بالخطوات التالية ، لقد استخدم الاسيتالديهيد كمثال توضيحي ونلاحظ أن الميكانيكية التالية تنطبق على أي الديهيد أو كيتون شرط احتوائه على ذرة ألفا - هيدروجين .
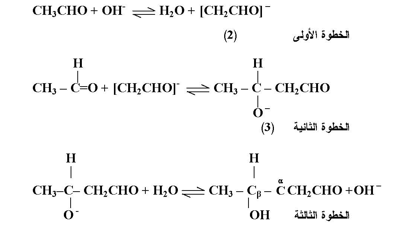
وتتضمن الخطوة الأولى سحب البروتون المتصل بذرة كاربون - ألفا وذلك بتأثير القاعدة لتوليد الأنيون الكاربوني المناظر (2) ( الذي يعمل كعامل نيوكليوفيلي ) ، والذي يهاجم ذرة كاربون مجموعة الكاربونيل ( لجزيئة أخرى غير متأثرة بالقاعدة ) ليعطي الأيون (3) علماً بأن الشحنة السالبة محمولة الآن على ذرة أوكسجين الالدول ، وهذا يعني أن (3) هو الكوكسيد .
وفي الخطوة الأخيرة يعمل أيون الالكوكسيد (3) على سحب بروتون من جزيئة الماء المتكونة في الخطوة الأولى أو المستخدمة كمذيب أي قاعدة مخففة ليعطي الناتج النهائي ، بيتا - هيدروكسي الديهيد ومعيداً تكوين القاعدة .
ومن الممكن إجراء نفس التفاعل ولكن باستخدام حامض كحافز والذي ميكانيكيته وبالطبع ستختلف عن ذلك المحفز بقاعدة مخففة وفيما يلي الخطوات والتي يتوقع بأن التفاعل المحفز بحامض سيمر من خلالها المعادلة التالية :
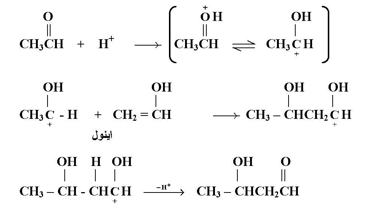
وتتضمن الخطوة الأولى إضافة البروتون على مجموعة كاربونيل الالديهيد ، يعقبها بخطوة منفصلة إضافة جزئية الالديهيد المضاف إليه بروتون على حالة الاينول لمركب الالديهيد ليعطي ناتج التكاثف والذي يفقد بروتوناً في خطوة منفصلة ليعطي الناتج النهائي .
ونجد أن مجموعة الكاربونيل لمركب الالديهيد لعبت في ميكانيكية التفاعل المحفز بقاعدة دورين مهمين في تكاثف الدول : الأول مساهمتها من خلال سحبها للالكترونات لجعل الهيدروجين ألفا ذا حامضية كافية بحيث يمكن سحب هذا النوع من البروتونات بقاعدة مخففة لتكوين الانيون الكاربوني ، أما التأثير الثاني فمساهمتها بتوفير المركز الذي حدثت عنده الإضافة .
أما في التكاثف المحفز حامضياً فإن الحامض لقد لعب دورين أولهما تحفيز تحول مركب الكاربونيل إلى أينوله وثانيهما توفير مركب الكاربونيل المضاف إليه بروتون والذي يمكن للأينول التفاعل معه بسهولة .