علم الكيمياء

تاريخ الكيمياء والعلماء المشاهير

التحاضير والتجارب الكيميائية

المخاطر والوقاية في الكيمياء

اخرى

مقالات متنوعة في علم الكيمياء

كيمياء عامة


الكيمياء التحليلية

مواضيع عامة في الكيمياء التحليلية

التحليل النوعي والكمي

التحليل الآلي (الطيفي)

طرق الفصل والتنقية


الكيمياء الحياتية

مواضيع عامة في الكيمياء الحياتية

الكاربوهيدرات

الاحماض الامينية والبروتينات

الانزيمات

الدهون

الاحماض النووية

الفيتامينات والمرافقات الانزيمية

الهرمونات


الكيمياء العضوية

مواضيع عامة في الكيمياء العضوية

الهايدروكاربونات

المركبات الوسطية وميكانيكيات التفاعلات العضوية

التشخيص العضوي

تجارب وتفاعلات في الكيمياء العضوية


الكيمياء الفيزيائية

مواضيع عامة في الكيمياء الفيزيائية

الكيمياء الحرارية

حركية التفاعلات الكيميائية

الكيمياء الكهربائية


الكيمياء اللاعضوية

مواضيع عامة في الكيمياء اللاعضوية

الجدول الدوري وخواص العناصر

نظريات التآصر الكيميائي

كيمياء العناصر الانتقالية ومركباتها المعقدة


مواضيع اخرى في الكيمياء

كيمياء النانو

الكيمياء السريرية

الكيمياء الطبية والدوائية

كيمياء الاغذية والنواتج الطبيعية

الكيمياء الجنائية


الكيمياء الصناعية

البترو كيمياويات

الكيمياء الخضراء

كيمياء البيئة

كيمياء البوليمرات

مواضيع عامة في الكيمياء الصناعية

الكيمياء الاشعاعية والنووية
الخواص الطبيعية للكحولات
المؤلف:
أ. د محمد مجدي واصل
المصدر:
اساسيات الكيمياء العضوية
الجزء والصفحة:
ص 297-298-299- 300
2023-08-20
1502
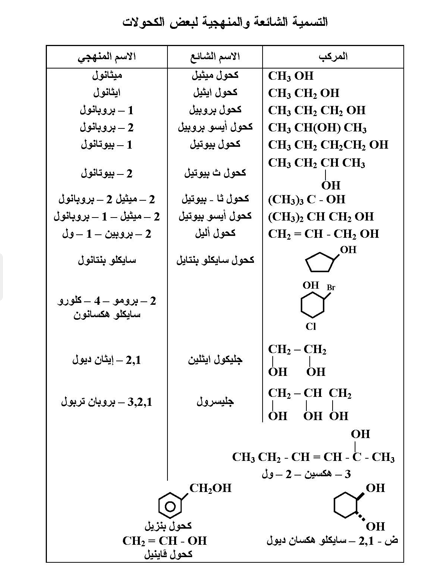
نجد أن الكحولات الأولى مواد سائلة ، ثم بعد ذلك نجد يصبح سوائل زيتية القوام ، وتتميز الكحولات بدرجات غليان عالية مقارنة بالألكانات والايثرات وهاليدات الألكيل المقارنة لها في الأوزان الجزيئية ، فدرجة غليان الميثانول - مثلاً - هي 65° م بينما الإيثان غاز . ويرجع ارتفاع درجات غليان الكحولات وكذلك الفينولات والأحماض الكربوكسيلية إلى ظاهرة الرابطة الهيدروجينية ، ففي الكحولات تتصل ذرة هيدروجين بجزيئ كحول بذرة أكسجين جزئ كحول آخر .
وهذه الرابطة الهيدروجينية عبارة عن تجاذب اليكتروستاتيكي يؤدي إلى تجمع الجزيئات لتكون جزيئيات أكبر تحفظها سوياً . وترتفع نتيجة لذلك درجات الغليان ، وتزيد الحاجة إلى طاقة أكبر لكسر هذا التجمع الذي لا يوجد مثله في الهيدروكربونات أو الايثرات .
ولقدرتها على إنشاء روابط هيدروجينية مع الماء ؛ فإن الكحولات الأولية C4-C1 تمتزج مع الماء بأية نسبة ، ويقل الامتزاج بعد ذلك بزيادة الوزن الجزيئي للكحول مثل كحول ديكابل C10 H21 OH لأنه عند ذلك يشبه هيدروكربون لطول سلسلته الكربونية .
وتتفاعل الكحولات كقواعد د تقبيلها بروتوناً من حمض قوي مثل حمض الكبريتيك أو الفوسفوريك ؛ متحولة بذلك إلى أيون أوكسونيوم :

كذلك تتفاعل الكحولات كأحماض عند تفاعلها مع فلز الصوديوم :

وهذا الجدول يبين الخواص الطبيعية لبعض الكحولات كما يلي :