

علم الكيمياء

تاريخ الكيمياء والعلماء المشاهير

التحاضير والتجارب الكيميائية

المخاطر والوقاية في الكيمياء

اخرى

مقالات متنوعة في علم الكيمياء

كيمياء عامة


الكيمياء التحليلية

مواضيع عامة في الكيمياء التحليلية

التحليل النوعي والكمي

التحليل الآلي (الطيفي)

طرق الفصل والتنقية


الكيمياء الحياتية

مواضيع عامة في الكيمياء الحياتية

الكاربوهيدرات

الاحماض الامينية والبروتينات

الانزيمات

الدهون

الاحماض النووية

الفيتامينات والمرافقات الانزيمية

الهرمونات


الكيمياء العضوية

مواضيع عامة في الكيمياء العضوية

الهايدروكاربونات

المركبات الوسطية وميكانيكيات التفاعلات العضوية

التشخيص العضوي

تجارب وتفاعلات في الكيمياء العضوية


الكيمياء الفيزيائية

مواضيع عامة في الكيمياء الفيزيائية

الكيمياء الحرارية

حركية التفاعلات الكيميائية

الكيمياء الكهربائية


الكيمياء اللاعضوية

مواضيع عامة في الكيمياء اللاعضوية

الجدول الدوري وخواص العناصر

نظريات التآصر الكيميائي

كيمياء العناصر الانتقالية ومركباتها المعقدة


مواضيع اخرى في الكيمياء

كيمياء النانو

الكيمياء السريرية

الكيمياء الطبية والدوائية

كيمياء الاغذية والنواتج الطبيعية

الكيمياء الجنائية


الكيمياء الصناعية

البترو كيمياويات

الكيمياء الخضراء

كيمياء البيئة

كيمياء البوليمرات

مواضيع عامة في الكيمياء الصناعية

الكيمياء الاشعاعية والنووية
الخواص الفيزيائية للأمينات
المؤلف:
أ. د محمد مجدي واصل
المصدر:
اساسيات الكيمياء العضوية
الجزء والصفحة:
ص 407-408-409
2023-08-27
2473
تعد الأمينات من المركبات القطبية ( Polar ) وعلى هذا الأساس فأن الأمينات عدا الثنائية يمكنها أن تُكون روابط هيدروجينية بينية ( Intermolecular hydrogen bonda ) وبهذا فأنها تشبه الأمونيا .
ولقد وجد أن الرابطة الهيدروجينية HN....N هي أضعف من الرابطة الهيدروجينية مع الأوكسجين OH....O وذلك بسبب كون ذرة النتروجين أقل سالبية من الأوكسجين ولهذا فأن رابطة NH هي أقل قطبية .
وينعكس عن هذه الرابطة الهيدروجينية الضعيفة بين جزيئات الأمين ارتفاع نسبي في درجات غليان الأمينات .ولقد وجد أن هذه الدرجات هي أعلى من درجات غليان المركبات التي لا يمكنها تكوين مثل هذه الروابط ( مثل الألكينات والأيثرات ) وأقل من درجات غليان المركبات القادرة على تكوين روابط هيدروجينية قوية ( كالكحولات ) والتي لها نفس الأوزان الجزيئية التقريبية .
ولما كانت الأمينات الثالثية لا تحتوي على رابطة NH فأنها سوف لا تستطيع أن تكون روابط هيدروجينية بينية في حالتها السائلة النقية , وعلى هذا الأساس فأن الأمينات الثالثية تمتلك درجات غليان أقل من مثيلاتها الأولية والثانوية .
وأنها مقاربة لدرجات غليان الألكينات ذات الأوزان الجزيئية المقاربة لها مثلاً :
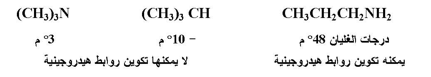
وتذوب جميع الأمينات ، والتي تملك الأوزان الجزيئية القليلة في الماء ويعود ذلك إلى قدرتها على تكوين روابط هيدروجينية مع الماء . ويمكن للأمينات الثالثية والأولية والثانوية أن تكون مثل هذه الروابط مع الماء .
ويرجع ذلك لاحتوائها جميعاً على زوج من الإلكترونات غير المشتركة الذي يستخدم في تكوين الروابط الهيدروجينية مع الماء . ولقد وجد أن قابلية ذوبان الأمينات في الماء تقل كلما زاد عدد ذرات الكاربون . كذلك فأن الأمينات تذوب في المذيبات الأقل قطبية كالأيثر والكحول والبنزين .
وتمتاز الأمينات الطيارة بأن لها روائح مزعجة مميزة فمثلاً للميثيل أمين رائحة تشبه رائحة الأمونيا ، ولثلاثي ميثيل أمين رائحة مشابهة لرائحة سمك السلامون ، بينما للبيريدين رائحة مشابهة لرائحة الأسماك الميتة والتي تعيش في المياه العذبة .
ولا تمتلك الأمينات الأريلية روائح غير مرغوب فيها مماثلة للأمينات الالكيلية ، إلا أنها جميعاً تعتبر مواد سامة ولها تأثيرات بايولوجية كونها تمتص من خلال الجلد . كما أن بعضها يعد مواد تسبب السرطان ، مثقل وتسلك أملاح الأمينات وأملاح الأمونيوم الرباعية سلوكاً يشبه الأملاح غير العضوية ، فجميعها عديمة الرائحة ، ذات درجات انصهار عالية ، وتذوب في الماء .