

علم الكيمياء

تاريخ الكيمياء والعلماء المشاهير

التحاضير والتجارب الكيميائية

المخاطر والوقاية في الكيمياء

اخرى

مقالات متنوعة في علم الكيمياء

كيمياء عامة


الكيمياء التحليلية

مواضيع عامة في الكيمياء التحليلية

التحليل النوعي والكمي

التحليل الآلي (الطيفي)

طرق الفصل والتنقية


الكيمياء الحياتية

مواضيع عامة في الكيمياء الحياتية

الكاربوهيدرات

الاحماض الامينية والبروتينات

الانزيمات

الدهون

الاحماض النووية

الفيتامينات والمرافقات الانزيمية

الهرمونات


الكيمياء العضوية

مواضيع عامة في الكيمياء العضوية

الهايدروكاربونات

المركبات الوسطية وميكانيكيات التفاعلات العضوية

التشخيص العضوي

تجارب وتفاعلات في الكيمياء العضوية


الكيمياء الفيزيائية

مواضيع عامة في الكيمياء الفيزيائية

الكيمياء الحرارية

حركية التفاعلات الكيميائية

الكيمياء الكهربائية


الكيمياء اللاعضوية

مواضيع عامة في الكيمياء اللاعضوية

الجدول الدوري وخواص العناصر

نظريات التآصر الكيميائي

كيمياء العناصر الانتقالية ومركباتها المعقدة


مواضيع اخرى في الكيمياء

كيمياء النانو

الكيمياء السريرية

الكيمياء الطبية والدوائية

كيمياء الاغذية والنواتج الطبيعية

الكيمياء الجنائية


الكيمياء الصناعية

البترو كيمياويات

الكيمياء الخضراء

كيمياء البيئة

كيمياء البوليمرات

مواضيع عامة في الكيمياء الصناعية

الكيمياء الاشعاعية والنووية
الخواص الفيزيائية للهاليدات
المؤلف:
د. محمد بن إبراهيم الحسن – د. حسن بن محمد الحازمي
المصدر:
أسس الكيمياء العضوية
الجزء والصفحة:
ص183-186
2025-01-11
93
الصفات الفيزيائية للهاليدات العضوية تتشابه سواء كانت أروماتية أو أليفاتية، وبسبب الوزن الجزيئي العالي للهالوجينات تجد أن درجة الغليان لها أعلى من الهيدروكربونات المماثلة لها من ناحية عدد ذرات الكربون. كما أن درجة الغليان تزداد بزيادة الوزن الجزيئي للهالوجين وذلك في حالة الهاليدات المتماثلة في المجموعة الألكيلية أو الأريلية حيث أن أيوديد الايثل يغلي عند 72م بينما يغلي. بروميد الايثل عند 38م. وبالرغم من أن الهاليدات العضوية تعتبر مركبات قطبية، بسبب الفرق في السالبية الكهربائية بين الكربون والهالوجين، إلا أنها لا تذوب في الماء، ربما يعزى ذلك إلى عدم قدرتها على تكوين روابط هيدروجينية مع الماء، إلا أنها تذوب في المذيبات العضوية.
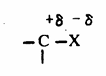
قطبية الرابطة بين الهالوجين والكربون : وتتميز الهاليدات العضوية خاصة التي فيها الهالوجين عبارة عن بروم أو يود أو عديد الكلور بأن لها كثافة أعلى من الماء.
طرق تحضير الهاليدات العضوية
أولاً : الهاليدات الألكيلية :
-1(هلجنة الهيدروكربونات الفصل الثاني)
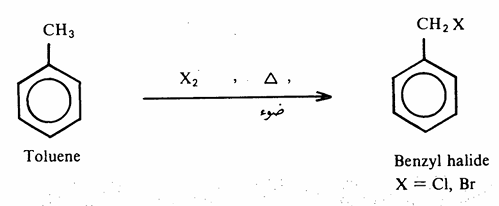
2 - إضافة هاليدات الهيدروجين للألكينات

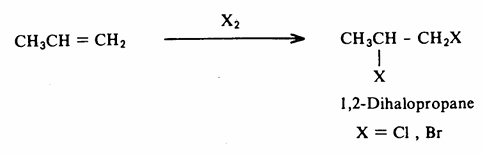
3- إضافة الهالوجينات للألكينات.
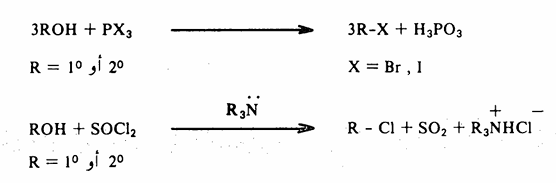
4- من الكحولات: يمكن أن يحل الهالوجين محل مجموعة الهيدروكسيل في الكحولات إما بمعاملة الكحولات بواسطة هاليد الهيدروجين أوهاليد الفسفور أو كلوريد ليونيل.

حيث ترتب فعالية هاليد الهيدروجين على النحو التالي: HCl<HBr<HIأما بالنسبة لـ HF فيعتبر غير فعال بشكل عام.
ثانياً : الهاليدات الأروماتية :
1 - الإستبدال الأروماتي الالكتروفيلي .
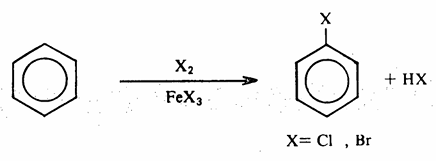
2 ـ عن طريق أملاح الديازونيوم وهي طريقة مهمة لتحضير العديد من الهاليدات الأروماتية .