علم الكيمياء

تاريخ الكيمياء والعلماء المشاهير

التحاضير والتجارب الكيميائية

المخاطر والوقاية في الكيمياء

اخرى

مقالات متنوعة في علم الكيمياء

كيمياء عامة


الكيمياء التحليلية

مواضيع عامة في الكيمياء التحليلية

التحليل النوعي والكمي

التحليل الآلي (الطيفي)

طرق الفصل والتنقية


الكيمياء الحياتية

مواضيع عامة في الكيمياء الحياتية

الكاربوهيدرات

الاحماض الامينية والبروتينات

الانزيمات

الدهون

الاحماض النووية

الفيتامينات والمرافقات الانزيمية

الهرمونات


الكيمياء العضوية

مواضيع عامة في الكيمياء العضوية

الهايدروكاربونات

المركبات الوسطية وميكانيكيات التفاعلات العضوية

التشخيص العضوي

تجارب وتفاعلات في الكيمياء العضوية


الكيمياء الفيزيائية

مواضيع عامة في الكيمياء الفيزيائية

الكيمياء الحرارية

حركية التفاعلات الكيميائية

الكيمياء الكهربائية


الكيمياء اللاعضوية

مواضيع عامة في الكيمياء اللاعضوية

الجدول الدوري وخواص العناصر

نظريات التآصر الكيميائي

كيمياء العناصر الانتقالية ومركباتها المعقدة


مواضيع اخرى في الكيمياء

كيمياء النانو

الكيمياء السريرية

الكيمياء الطبية والدوائية

كيمياء الاغذية والنواتج الطبيعية

الكيمياء الجنائية


الكيمياء الصناعية

البترو كيمياويات

الكيمياء الخضراء

كيمياء البيئة

كيمياء البوليمرات

مواضيع عامة في الكيمياء الصناعية

الكيمياء الاشعاعية والنووية
الايبوكسيدات (الأوكسيرينات) (Epoxides (Oxiranes
المؤلف:
د. محمد بن إبراهيم الحسن – د. حسن بن محمد الحازمي
المصدر:
أسس الكيمياء العضوية
الجزء والصفحة:
ص240-243
2025-01-14
49
هي ايثرات حلقية ثلاثية تسمى هذه المركبات ايبوكسيدات Epoxides إلا أنها تسمى بطريقة جنيف (IUPAC) أوكسيرينات Oxiranes.
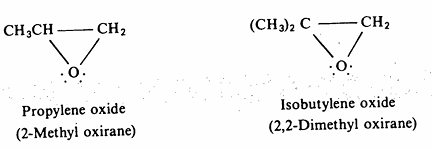
طرق التحضير :
1 ـ أكسدة الرابطة المضاعفة : يمكن الحصول على الايبوكسيد عن طريق أكسدة الرابطة المضاعفة بواسطة فوق أكاسيد الحموض مثل فوق أوكسيد حمض البنزويك Perbenzoic acid.
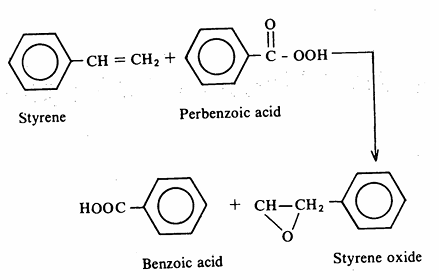
أما الصناعة فيمكن تحضير بعض الايبوكسيدات مثل أكسيد الايثيلين عن طريق الأكسدة بواسطة أكسجين الهواء الجوي في وجود عامل مساعد.
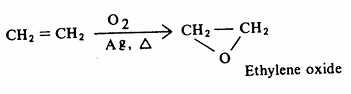
2- تحويل الهالوهيدرين إلى ايبوكسيد :
يمكن تحضير الهالوهيدرين من تفاعل الرابطة المضاعفة مع الماء والهالوجين (الكلور أو البروم) كما سبق وأن أوضحنا ذلك في تفاعلات الألكينات. يمكن تحويل الهالوهيدرين الناتج في وجود القاعدة إلى ايبوكسيد عن طريق إستبدال نيكليوفيلي داخلي (SN2) وهذا شبيه بتحضير وليمسون السابق للايثرات.
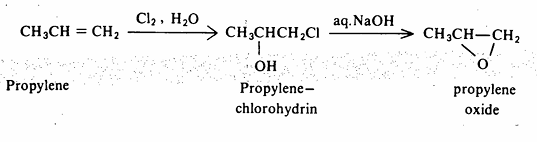
تفاعلات الايبوكسيد :
تتميز الايبوكسيدات بنشاط كيميائي مقارنة بالايثرات الأخرى وذلك لسهولة فتح الحلقة الثلاثية ذات الجهد الزاوي (راجع الألكانات الحلقية). فالايبوكسيدات تتفاعل بسهولة مع الحموض وكذلك مع القواعد على عكس الايثرات.
ا - تفاعلها مع الحموض . يتم تحويل الايبوكسيد إلى أيون الأكسونيوم Oxonium ion كما في حالة الايثرات يتفاعل أيون الأكسونيوم الناتج مع عدد كبير من النيكليوفيلات مثل الماء والكحول والفينول وغيرها.
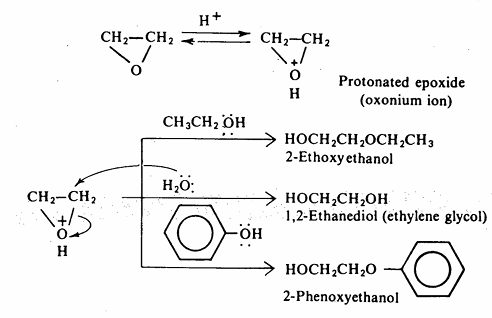
2- تفاعلها مع القواعد : تتفاعل الايبوكسيدات مع القواعد المختلفة مثل الأمونيا والأمينات وأيون الألكوكسيد والفينوكسيد عن طريق هجوم نيكليوفيلي.